 В августе 2021 г. французская Sanofi Pasteur выпустила на европейский рынок новую четырехвалентную противоменингококковую вакцину MenQuadf. Однако, помимо защищающих от менингококков серогрупп A, C, W-135 и Y, на рынке есть вакцины против менингококков групп С и В. В чем разница и какова практика иммунизации, принятая в разных странах?
В августе 2021 г. французская Sanofi Pasteur выпустила на европейский рынок новую четырехвалентную противоменингококковую вакцину MenQuadf. Однако, помимо защищающих от менингококков серогрупп A, C, W-135 и Y, на рынке есть вакцины против менингококков групп С и В. В чем разница и какова практика иммунизации, принятая в разных странах?
Менингококковая инфекция
Инвазивная менингококковая инфекция (ИМИ) — опасное для жизни заболевание, вызываемое бактерией Neisseria meningitidis . Наиболее яркими проявлениями ИМИ являются менингит и сепсис, но возможны и другие проявления. Начало заболевания — внезапное, с возможностью летального исхода в течение 24–48 ч после появления симптомов. У реконвалесцентов нередко наблюдают тяжелые и длительные осложнения.
Менингококк подразделяется на 12 серогрупп в зависимости от типа бактериального капсульного полисахарида. ИМИ чаще всего вызывают серогруппы A, B, C, W, X и Y. Заболеваемость менингококковой инфекцией наиболее высока у младенцев, за ней часто следует второй пик у подростков и молодых людей. Инфекция N. meningitidis поражает только людей при прямом контакте с респираторными каплями от инфицированного человека. Колонизацию носоглотки отмечают у 10% населения в целом (Pizza M. et al., 2020). Хотя носительство обычно протекает бессимптомно, оно может приводить к заболеванию. Образ жизни, включающий курение, поцелуи, посещение баров, пабов и ночных клубов, а также проживание в тесноте предрасполагает к носительству.
Вакцинация считается лучшей стратегией профилактики ИМИ, в том числе по причине стремительного течения болезни. Первые вакцины, основанные исключительно на капсульных полисахаридах против серогрупп A, C, W и Y, были полезными, но не очень эффективными для младенцев, имели короткую продолжительность защиты и не могли вызывать иммунную память. Разработка полисахаридно-конъюгированных менингококковых вакцин серогрупп A, C, W и Y (MenACWY) путем конъюгирования полисахаридного антигена с белком-носителем преодолела эти ограничения и позволила защитить детей раннего возраста, подвергающихся наиболее высокому риску. Кроме того, менингококковые конъюгированные вакцины позволили уменьшить или предотвратить носоглоточное носительство и, таким образом, обладали способностью вызывать коллективный иммунитет (Pizza M. et al., 2020).
Полисахаридные, конъюгированные и белковые
Первой вакциной для массовой иммунизации против менингококковой инфекции была VA-MENGOC-BC, разработанная кубинским государственным Институтом вакцин Финли (Instituto Finlay de Vacunas — IFV). Данная вакцина содержит полисахаридный компонент менингококка серогруппы С (MenC) и везикулы наружной мембраны группы В (MenВ) (Sierra-González V.G., 2020).
Основным недостатком полисахаридных вакцин является их неспособность продуцировать клетки памяти, что приводит к плохому ответу на бустер и короткой продолжительности защиты. Однако они очень эффективны в закрытых коллективах взрослых с высоким риском развития заболевания, в том числе военнослужащих и контактных на бытовом уровне (Ali A. et al., 2014). Из известных брендов называют полисахаридные вакцины Mencevax (GlaxoSmithKline) и Menomume (Sanofi Pasteur). Обе они защищают от серотипов A, C, W-135 и Y.
Конъюгированные вакцины были внедрены в 1999 г. в Великобритании (MenC). С тех пор конъюгированные четырехвалентные (A, C, W-135 и Y), двухвалентные C & Y и моновалентные вакцины MenA и MenС были одобрены в различных странах (табл. 1). После внедрения вакцинации в Великобритании заболеваемость в связи с MenC снизилась на 97% с 1998 г. Количество летальных исходов в связи с MenC уменьшилось с 78 в 1998 г. до 1 в 2008 г. (Sigurdardottir S.T., 2008). Сообщают, однако, что реакция памяти может быть недостаточно быстрой для защиты от менингококкового заболевания, обеспечивая в некоторых случаях лишь снижение его тяжести (Ali A. et al., 2014).
Полисахаридных вакцин MenВ не существует, их разрабатывали как белковые (см. ниже).
| Вакцина | Производитель | Серогруппы | Белковый конъюгат | Режим введения |
| Menactra | Sanofi Pasteur | A, C, W-135, Y | Дифтерийный токсин | FDA: детям 9–23 мес, по 2 дозы через 3 мес. Затем в возрасте 2–55 лет — еще 1 доза. Бустер возможен в возрасте 15–55 лет |
| Menveo | GSK Vaccines | A, C, W-135, Y | Дифтерийный олигосахарид CRM 197 | FDA: или в 2, 4, 6, и 12 мес, или начинают после 7 мес, причем 2-ю дозу вводят на 2-м году жизни спустя 3 мес после 1-й. Или одна доза в 2–55 лет. Бустер возможен: 15–55 лет
EMA: детям и взрослым с 2 лет. Мало данных относительно детей до 2 и лиц в возрасте старше 56 лет. Бустер возможен |
| Nemenrix | Pfizer/GSK | A, C, W-135, Y | Белок столбнячного токсина | ЕМА: дети с 6 мес до 6 лет 2 дозами через 2 мес. Дети с 6 мес и взрослые вакцинируются 1, но возможно и 2 дозами |
| MenQuadfi | SanofiPasteur | A, C, W-135, Y | Белок столбнячного токсина | FDA: дети с 2 лет — 1 доза. Бустер — с 15 лет.
ЕМА: дети с 12 мес — 1 доза. Бустер возможен. |
В 2005 г. первая четырехвалентная менингококковая конъюгированная вакцина (A, C, W-135, Y), конъюгированная с дифтерийным токсином (Menactra от Sanofi Pasteur), была одобрена Управлением по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA). Вторая вакцина Men ACWY, конъюгированная с CRM-197 (нетоксичный вариант дифтерийного токсина) (Menveo от GSK Vaccines), была одобрена ЕС и США в 2010 г., а Nemenrix от Pfizer/GSK — в 2012 г. в ЕС и Канаде.
Четвертая четырехвалентная вакцина
Итак, четвертая вакцина, защищающая от тех же четырех серотипов менингококка — MenQuadfi, одобрена в США (апрель 2020 г.) и ЕС (ноябрь 2020 г.). Почему четвертая, и есть ли между ними разница?
Активный ингредиент MenQuadfi (Sanofi Pasteur) представляет собой конъюгат капсульных полисахаридов групп A, C, W и Y со столбнячным анатоксином в качестве белка-носителя, который стимулирует выработку антител, специфичных к капсульному полисахариду. Как сообщает производитель, дизайн конъюгата разработан для каждого компонента в отдельности. В отличие от других четырехвалентных менингококковых вакцин, MenQuadfi поставляется в виде готового к использованию инъекционного раствора в ампуле, и его не нужно растворять перед инъекцией. В сравнительных исследованиях иммуногенности MenQuadfi vs Menveo и MenQuadfi vs Menactra у подростков и взрослых вакцина от Sanofi Pasteur показала как минимум не худшие, а в чем-то даже превосходящие результаты (www.menquadfi.com).
Вакцины против менингококка группы В
Вакцины для защиты от различных штаммов заболевания серогруппы B (MenВ) представляют проблему, поскольку полисахарид B обладает слабой иммуногенностью (Ali A. et al., 2014). Они обеспечивают непродолжительную защиту и требуют многократного введения. Новые вакцины, использующие субкапсульный белок, Trumenba (Wyeth Pharmaceuticals Inc., подразделение Pfizer Inc.) и BEXSERO (GSK Vaccines) получили в США ускоренное одобрение в 2014 и 2015 г. соответственно. В ЕС BEXSERO одобрена в 2013 г., а Trumenba — в 2017 г. Эти вакцины, основанные на циркулирующих в США штаммах, разрешены к применению у лиц в возрасте 10–25 лет, а BEXSERO в ЕС — у детей с 2-месячного возраста. Для прогнозирования регионального распространения штаммов Bexsero в разных странах используют Систему определения менингококкового антигена (Meningococcal Antigen Typing System — MATS) (Boccadifuoco G. et al., 2020).
Графики вакцинации
В США все дети в возрасте 11–12 лет должны получить конъюгированную вакцину против менингококка (A, C, Y, W) с бустерной дозой в 16 лет. Подростки и молодые люди (16–23 лет) также могут получить менингококковую вакцину серогруппы B. Центры по контролю и профилактике заболеваний (Centers for Disease Control and Prevention — CDC) также рекомендуют вакцинацию от менингококковой инфекции другим детям и взрослым, которые подвержены повышенному риску менингококковой инфекции.
На сегодня вакцины MenВ включены в государственные программы плановой иммунизации в Ирландии, Италии и Великобритании. Некоторые другие страны (Австрия, Чешская Республика и земля Саксония в Германии) рекомендовали вакцину без финансирования, а еще 6 предлагают ее только для групп риска.
Вакцины MenА сегодня используют в некоторых африканских странах (конъюгированные), а также, в комбинации с MenС, в Китае и Египте (полисахаридные) (Pizza M. et al., 2020). Куба и Новая Зеландия вакцинируют Men В и С, а большинство других стран — MenС (Австралия, страны ЕС, Великобритания).
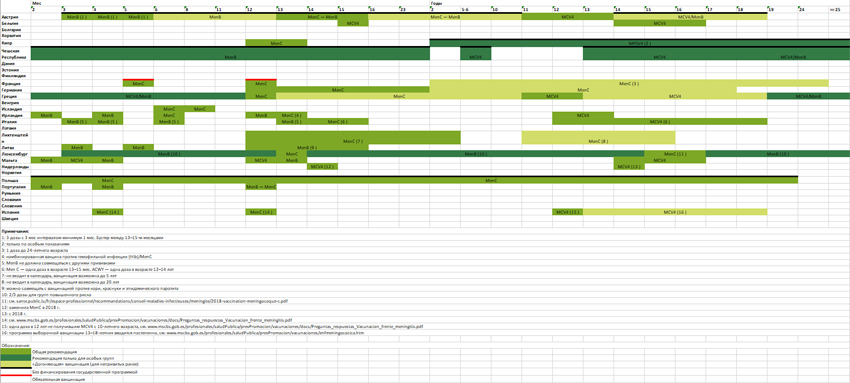
Более полная картина по странам — членам ЕС, где большинство случаев заболевания вызвано серогруппами B и C, выглядит следующим образом (табл. 2). Например, немецкий Институт Роберта Коха (Robert-Koch-Institut — RKI) рекомендует при повышенном риске возникновения менингококковых заболеваний (врожденные или приобретенные иммунные дефекты) вакцинировать менингококковой конъюгированной вакциной ACWY и менингококковой вакциной B детей и взрослых.
Список использованной литературы
- Ali A., Jafri R.Z., Messonnier N. et al. (2014) Global practices of meningococcal vaccine use and impact on invasive disease. Pathog Glob Health, 108(1): 11–20. doi:10.1179/2047773214Y.0000000126.
- Boccadifuoco G., Brunelli B., Mori E. et al. (2019) Meningococcal Antigen Typing System (MATS): A Tool to Estimate Global Coverage for 4CMenB, a Multicomponent Meningococcal B Vaccine. Methods Mol Biol, 1969: 205–215. doi: 10.1007/978-1-4939-9202-7_14. PMID: 30877679.
- Pizza M., Bekkat-Berkani R., Rappuoli R. (2020) Vaccines against Meningococcal Diseases. Microorganisms, 8(10): 1521. Published 2020 Oct 3. doi:10.3390/microorganisms8101521.
- Sierra-González V.G. (2020) Cuban Meningococcal Vaccine VA-MENGOC-BC®: 30 Years of Use and Future Potential. VacciMonitor, 29(1): 32–43.
- Sigurdardottir S.T., Davidsdottir K., Arason V.A. et al. (2008) Safety and immunogenicity of CRM197-conjugated pneumococcal-meningococcal C combination vaccine (9vPnC-MnCC) whether given in two or three primary doses. Vaccine. Aug 5; 26(33): 4178-86.
www.ema.europa.eu; www.fda.gov; www.rki.de

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим