У 2009 р., як і в попередні роки, спостерігається тенденція до зростання надходження повідомлень про ПР ЛЗ. Так, згідно з щорічною галузевою звітністю — форма 69, у закладах охорони здоров’я сталося 8640 випадків ПР ЛЗ. Інформацію про них надали 40,6% закладів охорони здоров’я. Після проведення аналізу отриманих карт-повідомлень до бази даних про ПР ЛЗ Управління Центру було введено 7242 карт-повідомлень про ПР ЛЗ належної якості з 37% закладів охорони здоров’я. Загалом рівень надходження повідомлень про ПР ЛЗ в Україні відповідає критеріям ВООЗ: 157 повідомлень на 1 млн населення.
Минулого року найбільш активно сповіщали про ПР ЛЗ лікарі АР Крим, Харківської, Вінницької, Луганської, Житомирської, Донецької областей та м. Києва. Надзвичайно низькою була активність лікарів Рівненської, Одеської та Сумської областей.
Найбільш часто ПР при медичному застосуванні ЛЗ спостерігалися при лікуванні ішемічної хвороби серця (8,95% повідомлень), гострих респіраторних вірусних захворювань (5,7%), гострого бронхіту (5,0%), гіпертонічної хвороби (4,7%), пневмонії (3,9%), психічних розладів (3,3%), туберкульозу (2,9%), хронічного обструктивного захворювання легень (2,6%), ВІЛ (2,3%), злоякісних новоутворень (2,2%).
Найбільш часто ПР виникали на тлі прийому протимікробних засобів для системного застосування, препаратів, які впливають на серцево-судинну, нервову системи (табл. 1, рис. 1). Перелік міжнародних непатентованих назв ЛЗ, при застосуванні яких ПР виникали найчастіше, очолюють цефтріаксон, декстран, амоксицилін у комбінації з ферментом (табл. 2).
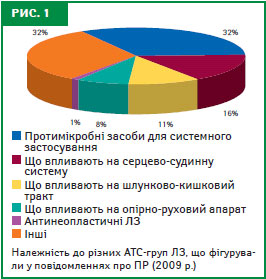
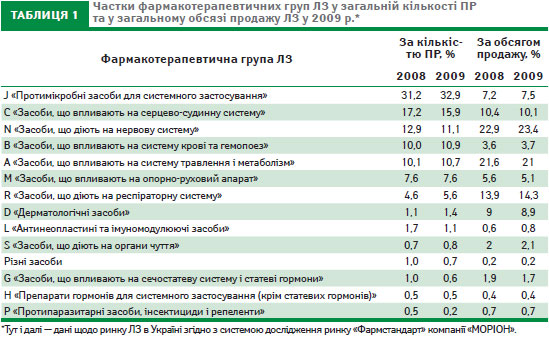
 Серед протимікробних засобів для системного застосування незрівнянно більша кількість повідомлень надійшла про ПР антибактеріальних засобів для системного застосування (75,8%), які у більшості випадків проявлялися алергічними ПР. Подальший аналіз показав, що найчастіше ПР виникали при застосуванні таких ЛЗ (за міжнародною непатентованою назвою): цефтріаксон (12,7%), амоксицилін у комбінації з клавулановою кислотою (8,2%), амоксицилін (6,6%).
Серед протимікробних засобів для системного застосування незрівнянно більша кількість повідомлень надійшла про ПР антибактеріальних засобів для системного застосування (75,8%), які у більшості випадків проявлялися алергічними ПР. Подальший аналіз показав, що найчастіше ПР виникали при застосуванні таких ЛЗ (за міжнародною непатентованою назвою): цефтріаксон (12,7%), амоксицилін у комбінації з клавулановою кислотою (8,2%), амоксицилін (6,6%).
Серед засобів, що впливають на серцево-судинну систему, повідомлення про ПР найчастіше надходили на препарати пентоксифіліну (12,5%), амлодипіну (8,0%) та еналаприлу (7,9%).
Серед засобів, що впливають на нервову систему, найбільша кількість повідомлень про ПР надійшла на галоперидол (7,4%), парацетамол (7,4%) та метамізол натрій (7,0%).
Серед засобів, що впливають на систему крові та гемопоез, найбільша кількість повідомлень про ПР надійшла на препарати декстрану (29,0%), електроліти та їх комбінації з іншими препаратами (21,3%), розчин натрію хлориду (7,3%).
Серед засобів, що впливають на опорно-руховий апарат, найбільша кількість повідомлень про ПР надійшла на диклофенак (31,9%), ібупрофен (12,1%) та німесулід (9,9%).
Серед засобів, що впливають на шлунково-кишковий тракт, найбільша кількість повідомлень про ПР надійшла про комбінації пітофенону з анальгетиками (8,1%), тіотріазолін (6,1%) та кислоту тіоктову (4,3%).
Для аналізу спонтанних повідомлень використовують також епідеміологічні методи. Зокрема за допомогою визначення такого показника, як частота репортування (ЧР — кількість повідомлень, поділена на кількість призначень або обсяг продажу), можна порівняти один з одним декілька препаратів (Brinker A., Beitz J., 2002). Вагому різницю у значеннях ЧР щодо аналогічних препаратів можна розглядати як одне зі свідчень проблем з безпекою окремих ЛЗ. Звичайно, на результативність такого підходу негативний вплив справляє низький рівень репортування, що є загальною проблемою, і навіть в США його оцінюють у 1–10% (GAO US, 2000). Застосування цього методу має й інші важливі обмеження із статистичної точки зору, тому використовують його лише як орієнтовний.
Так, за даними 2009 р., серед препаратів цефтріаксону є такий (його виробник зареєстрований у офшорній зоні), ЧР щодо якого у 20 разів вища середньої для цефтріаксонів. Ще у двох препаратів цефтріаксону (вітчизняного та азійського виробництва) цей показник у 18 та 17 разів вищий за середній. Вищезазначений виробник з офшорної зони постачає на український ринок препарат німесуліду, ЧР якого значно вища, ніж у інших препаратів німесуліду. Дещо нижчий показник має індійський препарат німесуліду. Також з Індії походить препарат амоксициліну/клавуланової кислоти, що є лідером за ЧР серед аналогічних. На порядок вище, ніж у інших, є ЧР у двох препаратів ібупрофену європейського виробництва. Серед препаратів диклофенаку лідером за показником ЧР є лікарський засіб індійського виробництва. Поміж препаратів пентоксифіліну два препарати індійського та європейського виробництва мали ЧР, майже вдвічі більшу, ніж середня. Нерівномірно розподілені ПР серед різних препаратів галоперидолу: індійський та український мають у 3–4 рази вищу ЧР, ніж європейський.
Представлені дані потребують більш глибокого вивчення та прийняття відповідних рішень, зокрема щодо подальшого медичного застосування.
За підсумками діяльності системи охорони здоров’я за 2009 р. (МОЗ України), у структурі захворюваності населення найбільша частка належить хворобам органів дихання та системи кровообігу (рис. 2).
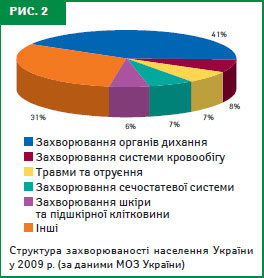
Нами була виявлена певна залежність при порівнянні кількості повідомлень про ПР відповідно до групової належності «винного» ЛЗ (за АТС) та фонового захворювання (за МКХ), із структурою захворюваності й поширеності хвороб (табл. 3).
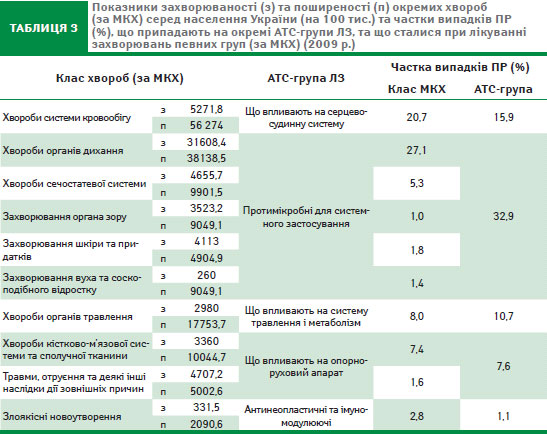
Так, у 2009 р. на 1-му місці за захворюваністю знаходилися хвороби серцево-судинної системи. Однак кількість повідомлень відносно ЛЗ, які застосовуються для лікування цієї патології, знаходиться на 2-му місці після протимікробних засобів для системного застосування (див. рис. 1). Поясненням цьому може бути використання протимікробних засобів при лікуванні хвороб різної приналежності за МКХ, так що сумарний показник захворюваності на них є у 8 разів вищим, ніж рівень захворюваності органів системи кровообігу. Тому питома вага випадків ПР на тлі прийому протимікробних засобів для системного застосування є найбільшою.
Між захворюваністю, частотою призначень ЛЗ та частотою інформування про ПР також прослідковується зв’язок (див. табл. 3). Менш чіткий зв’язок спостерігається між поширеністю захворювань, частотою призначень ЛЗ та частотою інформування про ПР. На нашу думку, це пояснюється тим, що показник захворюваності вираховується відповідно до кількості первинних випадків хвороб, які зазвичай потребують проведення фармакотерапії. Навпаки, поширеність стосується і хронічних хворих, які у період ремісії не потребують лікування.
За даними аналізу МОЗ України, за останні 5 років спостерігається підвищення захворюваності на окремі види серцево-судиної патології (гіпертонічну хворобу, ішемічну хворобу та цереброваскулярні захворювання), а також злоякісних новоутворень (раку передміхурової залози, нирки, щитоподібної залози, тіла матки, глотки та прямої кишки). Зважаючи на встановлений нами зв’язок, у подальшому не виключено зростання рівню надходження повідомлень про ПР ЛЗ на тлі захворювань, що вказані вище.
Проте частота застосування ЛЗ — не єдиний фактор, який впливає на частоту інформування про ПР. Надзвичайно важливим є профіль безпеки ЛЗ, тому закономірно очікувати на більш високий рівень репортування про ПР, наприклад, антинеопластичних засобів.
Певну невідповідність було виявлено між показниками захворюваності/поширеності хвороб та обсягом продажу ЛЗ відповідних класів (табл. 4, 5). Так, найвищі показники продажу мають далеко не ті ЛЗ, що належать до перших ліній лікування найбільш розповсюдженої в Україні патології (див. табл. 4). Навіть у групі ЛЗ, що впливають на серцево-судинну систему, на першому місці знаходяться препарати групи C01E X (різні комбіновані — Валідол, а не, скажімо, інгібітори АПФ (див. табл. 5).

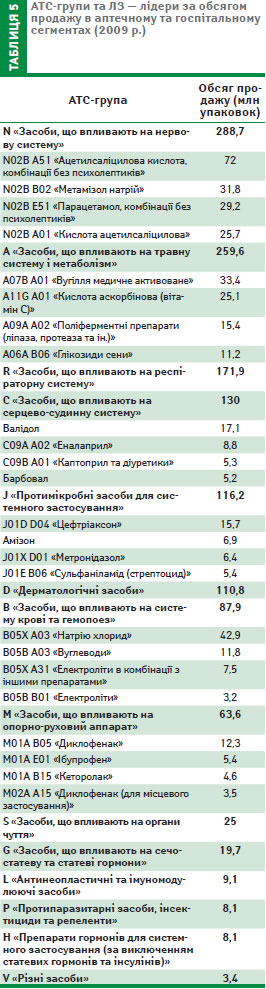 Така ситуація дає підстави вважати, що препарати застосовуються невідповідно до реальних потреб галузі, отже — нераціонально. Останнє вказує на необхідність впровадження в Україні Формулярної системи та її складової — моніторингу ефективності та безпеки ЛЗ стаціонарів закладів охорони здоров’я.
Така ситуація дає підстави вважати, що препарати застосовуються невідповідно до реальних потреб галузі, отже — нераціонально. Останнє вказує на необхідність впровадження в Україні Формулярної системи та її складової — моніторингу ефективності та безпеки ЛЗ стаціонарів закладів охорони здоров’я.
Як свідчить досвід інших країн, впровадження формулярної системи призводить до серйозного переформатування фармацевтичного ринку відповідно до потреб галузі охорони здоров’я, виходячи з вимог доказової медицини. Прикладом може бути Естонія, де за таким показником, як споживання у встановлених денних дозуваннях (Defined daily doses — DDD), серед АТС-груп лідерами є С, А, R та N (дані за 2008 р., State Agency of Medicines). При цьому серед ЛЗ групи С найбільше споживали аторвастатин, еналаприл, періндоприл та амлодипін; А — аскорбінову кислоту, омепразол, метформін та натрію фторид; R — ксилометазолін, сальбутамол, тимолол, теофілін; N — бетагістин, екстракт гінкго, цинаризин, альпразолам. Менші показники у DDD мають групи М, В, J та Н.
Залежно від країни виробництва ЛЗ кількість випадків ПР в нашій країні при застосуванні ЛЗ вітчизняного виробництва становила 44,2%, а іноземного — 55,8%. При цьому на Україну припадає 44,2%, Індію — 15,5%, Німеччину — 7,8%, Велику Британію — 4,3% випадків ПР. Ще декілька спостережень щодо особливостей виникнення ПР ЛЗ в Україні у 2009 р.
Залежно від країни — виробника ЛЗ у 2009 р. кількість випадків ПР розподілилася таким чином: на українські припало 44,2%, а зарубіжні — 55,8%. При цьому на Індію — 15,5%, Німеччину — 7,8%, Велику Британію — 4,3% випадків ПР.
Системними проявами ПР ЛЗ, інформація про які надійшла у 2009 р., найчастіше були алергічні реакції (60,58%), порушення з боку шлунково-кишкового тракту — у 10,97%, нервової системи — у 10,47%, серцево-судинні розлади спостерігалися у 7,81% випадків (табл. 6).
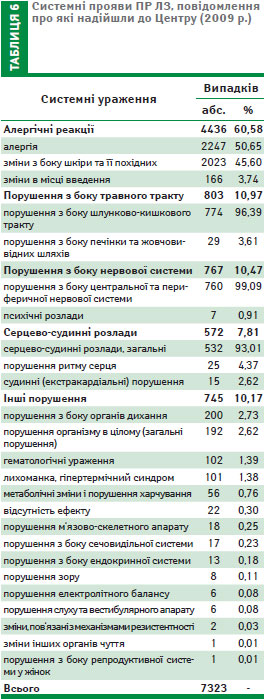
У більшості (60,6%) повідомлень про несприятливі наслідки ЛЗ будь-яких груп йшлося про алергічні ПР. Аналогічна ситуація була й у 2008 р. Переважно у повідомленнях не зазначалися дані алергологічного анамнезу, а проба на визначення підвищеної чутливості проводилася у такий спосіб, який у багатьох випадках не дозволяє оцінити індивідуальну чутливість пацієнта до ЛЗ. По-перше, відразу вводиться розведений у розчиннику ЛЗ, по-друге, використовують неоптимальні розведення, по-третє, відсутнє порівняння з гістаміном та негативною пробою, по-четверте, глибина введення не є стандартизованою. Такі помилки зазвичай призводять до: сенсибілізації організму до препарату, маніфестації алергічних ПР, хибнопозитивних оцінок або неможливості оцінити результати проб. Проте тільки при застосуванні прик-тестування не відбувається сенсибілізації організму до ЛЗ, та лише за наявності всіх складових (гістаміну, розчину тест-контролю, розчину ЛЗ та розчинника) можна об’єктивно оцінити наявність чи відсутність гіперчутливості.
При проведенні аналізу нами були розглянуті повідомлення про ПР ЛЗ на предмет медичних помилок. Так, серед отриманого у 2009 р. загалу повідомлень про ПР ЛЗ 2,4% випадків були наслідком медичних помилок. Найчастіше лікарями при призначенні препаратів не враховувалися протипоказання (49,7%), досить часто порушувався дозовий режим та спосіб введення ЛЗ (44,6%), дані анамнезу не були враховані у 3,4% випадків, несумісність застосування препаратів з іншими ЛЗ стала причиною виникнення ПР у 2,3% випадків.
Слід зазначити, що 98,8% ПР, інформація про які надійшла у 2009 р. до Центру, були передбаченими, тобто зазначеними в інструкції для медичного застосування ЛЗ, лише 1,2% ПР були непередбаченими, тобто на момент виявлення про них не було зазначено в інформації про ЛЗ. За результатами післяреєстраційного нагляду за достатньої кількості інформації та встановлення причинно-наслідкового зв’язку між ПР та застосуванням ЛЗ в інструкції для медичного застосування ряду ЛЗ у 2009 р. та на початку 2010 р. були внесені зміни та доповнення у розділ «Побічні реакції». Наприклад, через формування сигналу були внесені зміни щодо безпеки в інструкцію препарату L-лізину есцинат. Продовжується спостереження за ЛЗ, на які у післяреєстраційний період отримано не більше двох повідомлень про непередбачені ПР.
Більшість ПР (79,9%) були несерйозними, 20,1% — серйозними. Виникнення серйозних ПР у 43,1% випадках стало причиною госпіталізації пацієнтів; у 26,3% випадках призвело до тимчасової непрацездатності; у 25,1% випадків являло загрозу життю пацієнта; у 13,7% випадків ПР призвели до подовження терміну госпіталізації хворих; у 1,2% — ПР закінчилися летально.
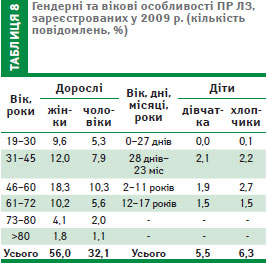
У жінок ПР спостерігалися в 1,7 раза частіше, ніж у чоловіків, що відповідає світовим тенденціям. Найбільшу кількість повідомлень про ПР ЛЗ як у чоловіків, так і у жінок, реєстрували у віковому проміжку від 31 до 60 років (44,4%). Як і в попередні роки, рівень інформування про ПР ЛЗ у дітей залишається низьким, що потребує негайних заходів з боку керівників лікувально-профілактичних закладів.
Причинно-наслідковий зв’язок між проявами ПР та застосуванням підозрюваних ЛЗ у 5,1% був достовірний, у 87,4% — вірогідний; у 7,3% — можливий; у 0,2% — сумнівний.
Протягом 2009 р. до Управління надійшло 14 повідомлень про летальні наслідки ПР у результаті медичного застосування ЛЗ. У всіх випадках було встановлено причинно-наслідковий зв’язок між ПР та застосуванням ЛЗ. Усі ПР були передбаченими, тобто про ймовірність їх виникнення було зазначено в інструкціях. У двох випадках причиною смерті стало застосування декількох препаратів (двох та трьох відповідно), в одному застосовувався комбінований ЛЗ, до складу якого входить дві діючі речовини (табл. 7).
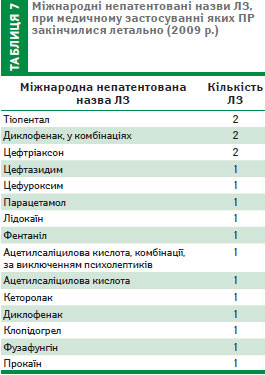
У 6 випадках летальні наслідки ПР виникли в результаті самолікування та допущених при цьому помилок. Серед них — тривале застосування НПЗП, їх комбінацій, парентеральне введення препаратів, у складі яких є місцеві анестетики, без попереднього визначення індивідуальної чутливості. Також у порядку самолікування двоє хворих застосовували комбінований препарат диклофенаку натрію та парацетамолу одночасно з фузафунгіном, що призвело до виникнення тяжких серйозних алергічних ПР. При цьому невідомо, чи було показано їм застосовувати ці препарати та яким був алергологічний анамнез.
Аналіз решти випадків летальних наслідків ПР показав таке. Декілька випадків сталися внаслідок анафілактичного шоку в результаті парентерального застосування антибіотиків цефалоспоринового ряду, лідокаїну гідрохлориду, тіопенталу натрію, фентанілу. Ще один випадок смерті стався в результаті тривалого застосування препарату клопідогрелу, який став причиною виникнення кишкової кровотечі, падіння артеріального тиску, геморагічного шоку.
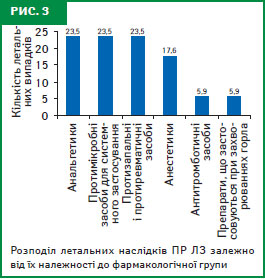
Загалом анальгетики, протимікробні засоби для системного застосування та НПЗП стали причиною летальних наслідків ПР у 23,5% відповідно, анестетики (місцеві та засоби для наркозу) — 17,6%, антитромботичні та препарати, що застосовуються при захворюваннях горла, — 5,9% кожні (рис. 3).
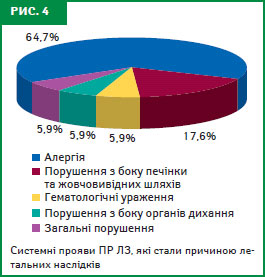
Летальні наслідки сталися через виникнення алергічних ПР у більшості випадків (64,7%). ПР, які проявлялися порушенням з боку печінки та жовчовивідних шляхів, були причиною смерті у 17,6% випадків, гематологічними ураженнями — у 5,9%, порушеннями з боку органів дихання — у 5,9%, порушення організму у цілому — 5,9% (рис. 4).
Залежно від країни виробництва ЛЗ, при застосуванні яких ПР закінчилися летально, розподілилися таким чином: 35% ЛЗ було вітчизняного виробництва, 17,65 — індійського, 5,9% — угорського, німецького, кіпрського та бангладешського, 23,5% — невідомого виробництва.
Аналіз повідомлень про летальні наслідки ПР дозволив виявити ще одну проблему застосування ЛЗ — наслідки безвідповідального самолікування. У 43% випадків летальні наслідки ПР були результатом саме помилок, які при цьому були допущені. Для попередження таких випадків у першу чергу слід розтлумачити потенційним споживачам ЛЗ правила застосування безрецептурних препаратів.
На основі результатів аналізу інформації про ПР протягом 2009 р. прийнято важливі регуляторні рішення щодо убезпечення подальшого медичного застосування в Україні деяких препаратів. Так, протягом 2009 р. було заборонено застосування в Україні:
- комбінованих препаратів, які містять німесулід і парацетамол резорбтивної дії (наказ МОЗ України від 04.06.2009 р. № 406);
- римонабанту (Акомплія) (наказ МОЗ України від 13.05.2009 р. № 318);
- ефалізумабу (Раптива) (наказ МОЗ України від 15.06.2009 р. № 512).
Також здійснення фармаконагляду дозволило впорядкувати, уніфікувати та затвердити інструкції на такі традиційні ЛЗ та інфузійні розчини:
- аміаку розчин, розчин для зовнішнього застосування 10%;
- кислота борна, розчин для зовнішнього застосування, спиртовий 3%;
- брильянтовий зелений, розчин для зовнішнього застосування, спиртовий 1%;
- водню пероксид, розчин для зовнішнього застосування 3%;
- етанол 70%, розчин;
- йод, розчин для зовнішнього застосування, спиртовий 5%;
- меновазин, розчин для зовнішнього застосування, спиртовий;
- метиленовий синій, розчин для зовнішнього застосування, спиртовий 1%;
- кислота саліцилова, розчин для зовнішнього застосування, спиртовий 1%;
- спирт камфорний, розчин для зовнішнього застосування, спиртовий 10%;
- спирт мурашиний, розчин для зовнішнього застосування, спиртовий;
- формідрон, розчин для зовнішнього застосування, спиртовий;
- розчин натрію хлориду 0,9%;
- розчин глюкози 5%;
- розчин глюкози 10%;
- розчин Рінгера;
- розчин Рінгера-лактату;
- розчин Реополіглюкіну.
Проведення аналізу інформації про ПР ЛЗ можна використовувати для побудови прогнозів щодо частоти виникнення ПР залежно від частоти застосування ЛЗ (відповідно до даних захворюваності з більшою точністю, та з меншою — відповідно до даних поширеності хвороб). Останнє дасть можливість, по-перше, забезпечити всіх лікарів базовими знаннями з питань безпеки ЛЗ. По-друге — цілеспрямовано забезпечити додатковою інформацією лікарів тих спеціальностей, що надають допомогу при лікуванні хвороб та станів, які або мають тенденцію до зростання або при лікуванні яких використовуються ЛЗ з високим показником співвідношення ризик/користь. На сьогодні це стосується лікування певних захворювань системи кровообігу та злоякісних новоутворень і застосування засобів, що впливають на серцево-судинну систему, та антинеопластичних ЛЗ.
Аналіз отриманих результатів дозволяє виявити ті ЛЗ, які є найбільш ризикованими з огляду на безпеку, у межах однієї фармакологічної групи з подальшим прийняттям відповідних рішень.
Отримані протягом 2009 р. дані стосовно безпеки застосування ЛЗ дозволили визначити групи ризику щодо призначення фармакотерапії (діти віком 2–11 років та дорослі, особливо жінки, віком 46–60 років).
Аналіз випадків ПР виявив типові медичні помилки, які стали причиною виникнення ПР ЛЗ, що дозволило спланувати подальшу роботу щодо їх усунення. Одним із запобіжних заходів є вдосконалення наказу МОЗ та АМН України щодо профілактики, виявлення та лікування медикаментозної алергії.
Результати проведеного аналізу показали, наскільки серйозними є несприятливі наслідки безвідповідального самолікування. Останнє зумовило необхідність активізації просвітницької роботи співробітників регіональних відділень Управління Центру з потенційними споживачами ЛЗ.
Роль та місце кожного з цих чинників потребує подальшого додаткового вивчення, що є можливим за умов розбудови системи фармаконагляду, зокрема за впровадження методу моніторингу стаціонару щодо ефективності та безпеки ЛЗ як елементу Формулярної системи.

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим