|
Современная медицина предъявляет высокие требования к анализу информации относительно эффективности и безопасности ЛС:
• необходимость критической оценки информации, предназначенной для практических врачей и руководителей здравоохранения;
• выбор системных подходов для принятия решений в медицине (лечебных, диагностических, управленческих и др.).
Достоверность клинических доказательств эффективности лекарственной терапии в значительной степени зависит от правильной организации КИ, методологии, а также адекватности методов, применяемых для анализа данных, полученных в результате таких исследований.
Традиционно принятый описательный анализ медицинской информации часто искажает оценку результатов. Альтернативным подходом, приобретающим все бўольшую популярность, является систематический анализ с использованием статистических методов анализа данных различных КИ (метаанализ) [1].
Принципы доказательной медицины, основанные на современных статистических подходах при планировании и проведении КИ, позволяют с учетом требований к результатам КИ нивелировать влияние таких во многом субъективных факторов, как интуиция и квалификация врача, мнения авторитетных экспертов, рекомендации популярных руководств и справочников на принятие клинических решений (более подробно об этом см. «Еженедельник АПТЕКА», № 24 (345) от 17 июня 2002 г.).
КАКАЯ ИНФОРМАЦИЯ ДОСТОВЕРНА?
Важный аспект доказательной медицины — определение степени достоверности данных КИ, то есть результатов, которые берут за основу при составлении систематических обзоров. Центр доказательной медицины в Оксфорде разработал определения степени достоверности представляемой информации:
A. Высокая достоверность — информация основана на результатах нескольких независимых КИ с совпадением результатов, обобщенных в систематических обзорах.
B. Умеренная достоверность — информация основана на результатах по меньшей мере нескольких независимых, близких по целям КИ.
C. Ограниченная достоверность — информация основана на результатах одного КИ.
D. Строгие научные доказательства отсутствуют (КИ не проводились) — утверждение основано на мнении экспертов.
КАК ОЦЕНИТЬ ДАННЫЕ КИ?
Зададимся вопросом: доверять или нет? Из приведенных примеров можно сделать вывод, что высокой степенью достоверности характеризуются КИ, проведенные в соответствии с определенными требованиями. Без применения современных статистических методов невозможно решить основную задачу, возникающую перед каждым экспериментатором: как провести эксперимент и обработать его результаты, чтобы при заданных ограничениях на затраты получить максимум достоверной информации [3].
С точки зрения математической статистики, КИ являются выборочными, то есть анализ данных осуществляется на основании предположения, что определенная выборка пациентов (на которой проводятся КИ) будет наиболее точно соответствовать всей совокупности всех пациентов, которым будут назначать исследуемый препарат в процессе его клинического применения.
Поскольку выводы, сделанные на основе результатов КИ, затем распространяются на всю совокупность пациентов с соответствующим заболеванием, то основными вопросами, которые необходимо решить при планировании КИ (с точки зрения математической статистики), являются [2]:
• обеспечение репрезентативности выборки всей генеральной совокупности (по размеру и структуре);
• устранение возможных источников систематических ошибок;
• выбор методов обработки данных, соответствующих поставленной цели и особенностям анализируемых данных.
Для того, чтобы результаты КИ были достоверными, необходимо тщательное планирование их проведения, особенно в части используемых дизайнов (планов экспериментов) и обработки полученных данных. Статистический анализ результатов является неотъемлемой частью КИ. Большое значение имеет принятие определенной статистической модели, которая адекватно отображала бы ситуацию и учитывала все ограничения реальной действительности. Не останавливаясь подробно на характеристике основных фаз КИ, подробно описанных в «Еженедельнике АПТЕКА», № 16 (337) от 22 апреля 2002 г., все же отметим, что ключевыми фазами КИ, с точки зрения определения доказательств эффективности и безопасности ЛС, являются III и IV фазы. Важным требованием к дизайну КИ в III и IV фазах, с точки зрения статистики, является репрезентативность выборки.
РЕПРЕЗЕНТАТИВНОСТЬ ВЫБОРКИ
Формирование выборок — важнейший, с точки зрения статистических методов, элемент КИ. От этого зависит, получите ли вы в итоге необходимую информацию, а также достоверна ли она. Основные требования, предъявляемые к выборке, — однородность и репрезентативность.
Выборка должна быть представительной (репрезентативной) и адекватно отражать свойства генеральной совокупности. Степень представительности выборки определяется способом организации ее формирования и объемом [5].
Под генеральной совокупностью подразумевают всю совокупность реально существующих объектов (в случае проведения КИ — всю совокупность пациентов с данным заболеванием). С помощью тех или иных методов из генеральной совокупности выделяется выборочная совокупность, на которой и проводятся КИ. В процессе клинического применения ЛС выводы, сделанные на основе результатов КИ, проведенных на выборочной совокупности, будут распространены на всю генеральную совокупность. Для того чтобы выводы, сделанные на основе выборочных наблюдений, можно было распространить на всю генеральную совокупность, важно перед формированием выборки тщательно и полно определить генеральную совокупность, а также способ (методику) извлечения выборки, то есть выборка должна быть репрезентативной [5].
Определение размера и структуры выборки
Изучаемая выборка должна быть репрезентативна генеральной совокупности. Это означает, что при формировании выборки из совокупности она должна соответствовать таким требованиям [2]:
1. Вид статистического распределения выборки должен соответствовать распределению генеральной совокупности (при наличии нескольких выборок все они должны принадлежать одной генеральной совокупности).
2. Величина выборки должна быть достаточна для отражения структуры генеральной совокупности.
Поскольку данная статья имеет обзорный характер, не будем приводить формулы для расчета объема выборки [7]. Основным итогом можно считать то, что для получения достоверных результатов КИ необходимо наличие достаточного количества испытуемых.
Размер выборки
Для обеспечения получения надежных результатов количество пациентов, участвующих в КИ, всегда должно быть достаточно большим. Каким? Конкретный размер выборочной совокупности обычно определяется с учетом основной задачи КИ [7]. При установлении других критериев размера выборки необходимость этого шага нужно четко обосновать и указать в протоколе КИ. Например, если размер выборки для КИ определять на основе требований безопасности либо других важных, но второстепенных целей, он будет больше по сравнению с размером выборки для КИ, расчет которого основывается преимущественно на необходимости доказать эффективность [2].
СКОЛЬКО ЖЕ НУЖНО ПАЦИЕНТОВ?
Чтобы оценить порядок числа, характеризующего количество участников КИ, которые можно признать достоверными, рассмотрим график.
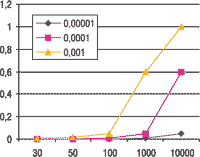 |
График. Вероятность обнаружения побочного эффекта в зависимости от размера выборки и его распространенности [3]
При малой выборке (а тем более еще и нерепрезентативной) вероятность обнаружить некий побочный эффект очень мала. Так, если изучаемый побочный эффект отмечают с частотой 1:10 000, то при проведении КИ с участием 30 пациентов вероятность обнаружить его хотя бы у одного практически отсутствует. Кроме того, вероятность обнаружения этого эффекта может еще больше уменьшиться вследствие того, что выборка нерепрезентативна.
Вероятность обнаружения побочного эффекта в КИ зависит как от размера выборки, так и от его распространенности. Таким образом, чем более редкий побочный эффект лекарственного препарата мы исследуем, тем больший размер выборки может повысить чувствительность исследования. Для получения надежных результатов КИ необходимо, чтобы количество участников эксперимента составляло около 10 000.
Означает ли все изложенное, что КИ, в которых принимает участие относительно небольшое количество пациентов, не нужны? Вовсе нет, такие исследования имеют определенное значение в рамках поставленных, как правило, ограниченных задач. Оценивать возможность их применения ко всей генеральной совокупности следует с определенной долей скепсиса, принимая во внимание, что чем меньше пациентов принимают участие в КИ, тем больше вероятность ошибки. Таким образом, наша задача — критично относиться к их результатам помня, что ориентируясь на величину выборки и ее репрезентативность и др., можем с известной степенью точности предполагать достоверность представляемых данных. Каждый читатель уполномочен на это своим образованием, профессией [6].
Денис Сухинин
|
ЛИТЕРАТУРА |
|
|

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим