|
З доповіддю на засіданні колегії виступив заступник міністра охорони здоров’я — голова Державної служби лікарських засобів і виробів медичного призначення Михайло Пасічник.
Він нагадав присутнім, що на Державну службу, яка є органом державного управління, покладено функції державного регулювання та контролю лікарських засобів і виробів медичного призначення. Свою діяльність Державна служба розпочала 23 жовтня 2003 р., після ліквідації Державного департаменту, тобто фактично вона працює три місяці.
ФАРМАЦЕВТИЧНИЙ РИНОК
|
М. Пасічник охарактеризував основні показники фармацевтичного ринку України у 2003 р. За підсумками 2003 р. обсяг внутрішнього ринку лікарських засобів збільшився на 27,4% і складає 4,9 млрд грн. Значно збільшилася частка імпортної продукції (в грошовому вираженні), що зумовлено як зростанням курсу євро, загрозою введення ПДВ на лікарські засоби наприкінці минулого року, а також змінами в структурі імпорту. За даними Державної митної служби, імпорт фармацевтичної продукції минулого року склав майже 600 млн дол. США, що на 40% більше, ніж у 2002 р.* Понад 40% імпорту надходить з Німеччини, Франції та Індії. В Україні зареєстровано понад 9 тис. лікарських засобів, з них 33,1% вітчизняних. Вартим уваги у цьому відношенні є аналіз структури і темпів реєстрації лікарських засобів трьох згаданих країн в Україні (рис. 1).
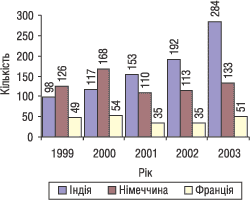 |
Рис. 1. Динаміка реєстрації лікарських засобів провідних країн-імпортерів
Експорт фармацевтичної продукції у минулому році склав 54,1 млн дол. США, що на 26% більше порівняно з 2002 р.*
У 2003 р. вітчизняними фармацевтичними підприємствами вироблено продукції на суму 2 млрд 30 млн грн.**, індекс виробництва склав 112,1%. Провідними виробниками ліків в Україні є Фармацевтична фірма «Дарниця» (13,0% загального обсягу вітчизняного виробництва у грошовому вираженні), «Фармак» (10,1%), «Фармацевтична компанія «Здоров’я» (9,5%), «Київмедпрепарат» (9,1%), «Борщагівський ХФЗ» (8,3%), «Індар» (4,7%). Частка інших 176 підприємств у загальному обсязі виробництва становить 45,3% (рис. 2).
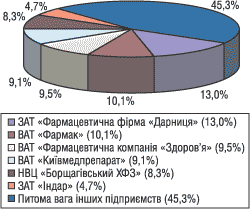 |
Рис. 2. Питома вага найпотужніших підприємств — виробників лікарських засобів за обсягом виробництва у 2003 р.
ЕКОНОМІЧНА ДОСТУПНІСТЬ ТА ПДВ
Далі М. Пасічник зупинився на основних засадах Національної політики щодо лікарських засобів, зокрема гарантуванні однакового доступу різних соціальних груп населення до основних лікарських засобів при їх фізичній та економічній доступності, що лягло в основу розроблення Державної програми забезпечення населення лікарськими засобами, затвердженої Кабінетом Міністрів. Фізична доступність забезпечується достатнім асортиментом лікарських засобів та розгалуженою мережею аптечних закладів. Щодо економічної доступності, то слід перш за все згадати перипетії, пов’язані з введенням ПДВ на лікарські засоби. Ця проблема виникла ще влітку минулого року, коли Верховною Радою України були прийняті зміни до податкового законодавства, яким передбачалося введення ПДВ на ліки. Завдяки принциповій позиції Президента України, який наклав вето на цей закон, вдалося уникнути подорожчання лікарських засобів в Україні. Потім Законом України «Про Державний бюджет України на 2004 рік» знову було передбачено введення ПДВ на медикаменти та вироби медичного призначення, крім тих, що входять до переліку, який затверджується урядом. М. Пасічник підкреслив, що під час підготовки проекту Державного бюджету на 2004 р. Міністерство охорони здоров’я неодноразово застерігало стосовно негативних наслідків введення ПДВ на лікарські засоби. На вирішення цієї проблеми було спрямовано Указ Президента України «Про невідкладні заходи щодо забезпечення права громадян на охорону здоров’я і медичну допомогу». На виконання цього указу урядом було прийнято рішення, за яким звільнялися від сплати ПДВ всі зареєстровані лікарські засоби та вироби медичного призначення згідно з переліком.
Якщо проблему з ПДВ на зареєстровані лікарські засоби вдалося вирішити, то проблема звільнення від сплати ПДВ лікарських засобів, які виготовляються аптечними закладами за рецептами лікарів та на замовлення лікувально-профілактичних закладів, залишилася. Державна служба звернулася до Міністерства юстиції з проханням надати з цього приводу офіційні роз’яснення. Також підготовлено проект рішення Кабінету Міністрів, яким передбачено врегулювання зазначеної проблеми.
Випереджаючи запитання щодо забезпечення виробництва ліків спиртом етиловим, М. Пасічник зазначив, що механізм компенсації додаткових витрат на спирт етиловий, який запропонував Мінфін, не спрацьовує (прим. ред. — в день проведення засідання колегії Верховна Рада України прийняла Закон України «Про внесення змін до деяких законодавчих актів України у зв’язку із прийняттям Закону України «Про Державний бюджет України на 2004 рік», яким на спирт етиловий, що використовується закладами та установами охорони здоров’я для забезпечення лікувально-діагностичного процесу і виконання лабораторних досліджень, а також суб’єктами підприємницької діяльності для виготовлення лікарських засобів, ставка акцизного збору встановлена в розмірі 2,0 грн. за 1 л 100-відсоткового спирту).
ОСНОВНІ ЛІКАРСЬКІ ЗАСОБИ
Важливою ділянкою роботи Державної служби була і буде надалі активна участь в оптимізації системи відбору та використання лікарських засобів, зазначив голова Державної служби. Першим кроком у цьому напрямі є оновлення переліку основних лікарських засобів відповідно до світового досвіду, на якому грунтуються рекомендації ВООЗ. Згідно з визначенням ВООЗ, основні лікарські засоби — це ті, «що задовольняють потребу більшості населення і повинні бути доступними для нього у будь-який час, у адекватній кількості, відповідних лікарських формах, а також мати ту вартість, яку може сплатити пацієнт і суспільство».
Протягом останніх місяців Державна служба спільно з головними спеціалістами МОЗ, представниками професійних громадських організацій, науковцями ініціювала розроблення проекту Національного переліку основних лікарських засобів замість Національного переліку основних (життєво необхідних) лікарських засобів і виробів медичного призначення. Підготовленим проектом зокрема передбачено:
•?включення лікарських засобів до переліку, насамперед, з урахуванням можливості їх застосування для лікування більшої частини населення України;
•?формування переліку як основи для закупівлі лікарських засобів за рахунок коштів державного та місцевих бюджетів;
•?виключення з переліку виробів медичного призначення;
•?приведення змісту переліку у відповідність з останніми рекомендаціями ВООЗ.
Важливо підкреслити, що перелік буде єдиним нормативним документом для закупівель за кошти державного бюджету. Ціни на лікарські засоби, включені до Національного переліку, будуть підлягати державній реєстрації. Важливою і, на жаль, «довгограючою» проблемою є запровадження системи державної реєстрації цін на лікарські засоби. Вирішується вона вже не перший рік. Але на сьогодні відсутній відповідний нормативно-правовий акт, який би регулював цю проблему. Міністерством охорони здоров’я та Державною службою вже підготовлено проект постанови Кабінету Міністрів України «Про затвердження Порядку державної реєстрації (перереєстрації) відпускних цін виробників (митної вартості) на лікарські засоби та вироби медичного призначення», який подано на розгляд відповідних центральних органів виконавчої влади.
Прийняття такої постанови дозволить:
•?забезпечити державний контроль за цінами на ліки, які підлягають державному регулюванню, не допустити їх істотного підвищення;
•?створити сприятливі умови для поліпшення забезпечення закладів охорони здоров’я та населення якісними, високоефективними, безпечними та доступними медикаментами;
•?врахувати рекомендації ВООЗ щодо підвищення економічної доступності ліків.
ВИРОБНИЦТВО НОВИХ ЛІКАРСЬКИХ ЗАСОБІВ
У 2003 р. підприємствами галузі розроблено 118 нових препаратів у різних формах, у тому числі 10 оригінальних за складом та 108 препаратів-генериків. Слід відзначити розвиток «заводської» фармацевтичної науки та створення наукових центрів з розроблення та впровадження нових лікарських засобів, які уже зараз діють на базах «Борщагівського ХФЗ», «ІнтерХіму», «Фармака», «Фарма Старту» та деяких інших. Таке поєднання є запорукою інтенсивного впровадження продукції, яка б замінила імпортну.
ВИРОБИ МЕДИЧНОГО ПРИЗНАЧЕННЯ
В Україні зареєстровано близько 3,5 тис. виробів медичного призначення, у тому числі в 2003 р. — 1138; з них 155 — вітчизняного і 983 — зарубіжного виробництва (рис. 3). Державна служба веде Державний реєстр виробів медичного призначення, дозволених до застосування в медичній практиці. Готується його перше офіційне видання, а електронну версію розміщено на офіційній web-сторінці Державної служби (цікавий факт — всього за 2 міс роботи кількість відвідувань сайту перевищило 25 тис. користувачів, що свідчить про ефективність такої форми висвітлення роботи Державної служби та встановлення інтерактивної комунікації з фахівцями галузі).
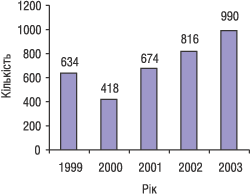 |
Рис. 3. Кількість зареєстрованих виробів медичного призначення (1999-2003 рр.)
На відміну від лікарських засобів, нормативне регулювання у сфері обігу виробів медичного призначення практично відсутнє (за винятком наказу «Про державну реєстрацію виробів медичного призначення» Міністерства охорони здоров’я). Саме тому Державна служба насамперед зосередила свої зусилля на розробленні проекту Закону України «Про вироби медичного призначення» та проекту постанови Кабінету Міністрів України щодо державної реєстрації виробів медичного призначення. Нагальність прийняття таких документів пов’язана з необхідністю забезпечення населення України безпечними й ефективними виробами, тим більше, що досі в Україні діють стандарти 90-х років, положення багатьох із них вже не відповідають сьогоденню та потребують перегляду.
ІМУНОБІОЛОГІЧНІ ПРЕПАРАТИ
На сьогодні в Україні зареєстровано 354 медичних імунобіологічних препарати (МІБП), з них 38% — вітчизняного виробництва. За 2003–2004 рр. (станом на 20 січня 2004 р.) було видано 58 підтверджень державної реєстрації медичних імунобіологічних препаратів та 74 висновки на відповідність медичного імунобіологічного препарату показникам якості (рис. 4, табл. 1).
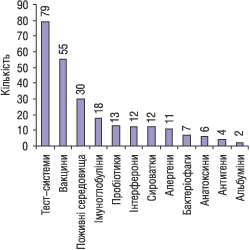 |
Рис. 4. Співвідношення зареєстрованих МІБП за основними групами
Таблиця 1
Динаміка кількості зареєстрованих МІБП
за основними групами по роках
|
Група МІБП |
2000 |
2001 |
2002 |
2003 |
|
Вакцини |
4 |
10 |
24 |
17 |
|
Тест-системи |
7 |
25 |
12 |
35 |
|
Поживні середовища |
8 |
12 |
5 |
5 |
|
Анатоксини |
0 |
2 |
2 |
2 |
|
Алергени |
2 |
5 |
1 |
3 |
|
Альбуміни |
0 |
1 |
0 |
1 |
|
Антигени |
0 |
3 |
1 |
0 |
|
Пробіотики |
0 |
5 |
3 |
5 |
|
Імуноглобуліни |
0 |
3 |
6 |
9 |
|
Інтерферони |
4 |
0 |
5 |
3 |
|
Бактеріофаги |
0 |
1 |
6 |
0 |
|
Сироватки |
0 |
1 |
7 |
4 |
Серйозною проблемою є застосування в медичній практиці незареєстрованих діагностичних систем. За оцінками фахівців, лише в закладах системи охорони здоров’я у більшості випадків використовуються саме такі діагностикуми. Це пов’язано з їх вузьким спектром застосування з одного боку, та порівняно високим державним збором за реєстрацію — з іншого. Для вирішення цієї проблеми Державною службою підготовлено відповідний проект постанови Кабінету Міністрів про реєстрацію таких препаратів, який зараз узгоджується відповідними центральними органами виконавчої влади.
ЛІЦЕНЗУВАННЯ ФАРМАЦЕВТИЧНОЇ ДІЯЛЬНОСТІ
Роздрібна, оптова торгівля лікарськими засобами, а також виробництво в умовах аптеки. Станом на 1 січня 2004 р. нараховується 5,5 тис. ліцензіатів. Загальна кількість точок роздрібної торгівлі медикаментами (аптек та їх структурних підрозділів) становить майже 22 тис., оптової — майже 1,5 тис. (рис. 5–6).
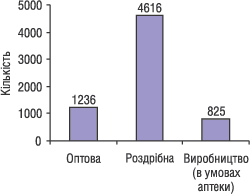 |
Рис. 5. Суб’єкти господарської діяльності, які мають ліцензію на провадження відповідного виду діяльності (на 01.01.2004)
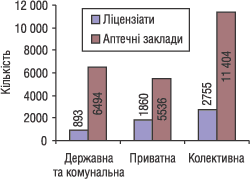 |
Рис. 6. Розподіл ліцензіатів та їх аптечних закладів за формою власності на 01.01.2004
|
Процедуру ліцензування нині спрощено. Це скоротило термін збору документів та кількість звернень до органу ліцензування з метою отримання ліцензії, дало змогу запобігти надмірному витрачанню коштів суб’єктами господарювання. Водночас зросла відповідальність самого суб’єкта за достовірність даних, що подаються в документах. Але спрощення процедури не повинно привести до вседозволеності у сфері обігу лікарських засобів. Ліцензування — це не формальна видача ліцензій на відповідний вид діяльності, а й чіткий контроль за дотриманням ліцензіатом ліцензійних умов у встановленому порядку, як визначено спільними наказами МОЗ та Держпідприємництва від 27 січня 2004 р. № 03/41 та 04/42, зареєстрованими в Міністерстві юстиції. До складу Ліцензійної комісії вперше увійшли представники Міністерства внутрішніх справ України, Служби безпеки України, громадських та професійних організацій. Результати роботи Ліцензійної комісії (рис. 7–9) висвітлюються в засобах масової інформації та на інтернет-сайті Державної служби.
Нагальною потребою сьогодення М. Пасічник назвав внесення змін до Ліцензійних умов. Також необхідно переглянути норму щодо функціонування аптечних кіосків. На думку доповідача, час, коли аптечні кіоски масово відкривалися, минув: слід приділяти увагу якості надання фармацевтичної допомоги. Тому внесення змін до правил роздрібної торгівлі лікарськими засобами — одне з першочергових завдань.
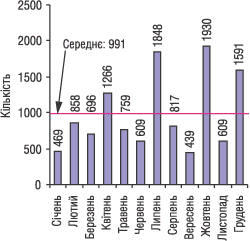 |
Рис. 7. Оформлено копій ліцензій на провадження господарської діяльності з оптової та роздрібної торгівлі лікарськими засобами за 2003 р.
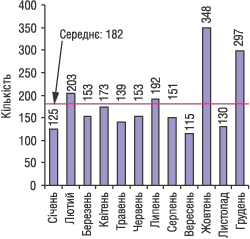 |
Рис. 8. Оформлено ліцензій (нових, переоформлених та дублікатів) на провадження господарської діяльності з оптової та роздрібної торгівлі лікарськими засобами за 2003 р.
У 2003 р. середній показник кількості населення України на один аптечний заклад (аптека, аптечний пункт та кіоск) склав 2200 осіб. Аналіз стану аптечної мережі в регіонах України свідчить, що навантаження на один аптечний заклад у містах становить від 1000 (у Чернігівській області) до 3000 осіб (у Чернівецькій області). Натомість навантаження на один аптечний заклад у сільській місцевості становить від 2000 у Закарпатській області до 12 000 осіб в Одеській. Це свідчить про необхідність вирішення проблеми розвитку сільської аптечної мережі шляхом перегляду вимог до обов’язкового складу та площ приміщень, кваліфікації персоналу, але з суворим дотриманням умов зберігання та відпуску ліків.
Обіг наркотичних засобів, психотропних речовин і прекурсорів. В Україні налічується майже 1700 суб’єктів господарювання, які мають ліцензії на обіг наркотичних засобів, психотропних речовин і прекурсорів. В 2003 р. такі ліцензії отримали 959 суб’єктів господарської діяльності.
Виробництво лікарських засобів. Державною службою постійно здійснюється визначення спроможності суб’єкта господарювання виконувати ліцензійні умови щодо виробництва лікарських засобів; на сьогодні ліцензовані 182 виробники лікарських засобів. Жодна ліцензія на виробництво лікарських засобів не була видана без попереднього обстеження матеріально-технічної бази виробника. Так, впродовж 2003 р. здійснено 60 таких перевірок, половина з них — Державною службою.
ЗАБЕЗПЕЧЕННЯ ЯКОСТІ
Одним із основних напрямів подальшого розвитку вітчизняної фармацевтичної галузі залишається забезпечення якості, безпеки та ефективності лікарських засобів. Єдиним шляхом виконання цього завдання є впровадження системи забезпечення якості, яка охоплює всі етапи обігу ліків від створення на основі формування попиту до реалізації та застосування кінцевим споживачем.
|
Основною складовою частиною системи забезпечення якості лікарських засобів є виробництво відповідно до вимог GMP. Якщо в Росії 14 липня 2003 р. було видано перший сертифікат відповідності виробництва державним стандартам ISO, що на думку МОЗ Росії, є першим етапом на шляху сертифікації за GMP, то в Україні за минулий рік видано сертифікати про повну відповідність GMP семи виробничим дільницям на п’яти фармацевтичних підприємствах («Борщагівський ХФЗ», «Фармацевтична фірма «Дарниця», «Фармак», «Індар» і «Фарма Старт»). Номенклатура лікарських засобів, виробництво яких здійснюється на сертифікованих дільницях, складає 48 найменувань (табл. 2). Наступним кроком повинне стати визначення обов’язковості правил GMP (безперечно, в першу чергу для найбільш критичних груп лікарських засобів, наприклад, стерильних лікарських форм, антибіотиків тощо).
Таблиця 2
Сертифікація виробничих дільниць вітчизняних підприємств-виробників лікарських засобів
на відповідність вимогам належної виробничої практики станом на 01.02.2004 р.
|
№ з/п |
Підприємство, виробнича дільниця |
№ сертифікату, термін дії |
Кількість найменувань лікарських засобів, виробництво яких здійснюється на дільниці |
|
1 |
ЗАТ НВЦ «Борщагівський ХФЗ» |
? |
? |
|
1.1 |
• стерильні порошки антибіотиків у флаконах |
№ 1/1, до 29.08.05 |
3 |
|
1.2 |
• нестерильні антибіотики в капсулах |
№ 2/1, до 29.08.05 |
7 |
|
1.3 |
• таблетки і капсули |
№ 6, до 29.08.05 |
16 |
|
2 |
ЗАТ «Індар» |
? |
? |
|
2.1 |
• готові лікарські засоби інсулінів |
№ 3, до 04.04.04 |
11 |
|
3 |
ВАТ «Фармак» |
? |
? |
|
3.1 |
• таблетки |
№ 4/1, до 26.12.05 |
2 |
|
4 |
ЗАТ «Фармацевтична фірма «Дарниця» |
? |
? |
|
4.1 |
• стерильні антибіотики для виготовлення розчинів для ін’єкцій у флаконах |
№ 5, до 25.05.05 |
3 |
|
5 |
ТОВ «Фарма Старт» |
? |
? |
|
5.1 |
• таблетки |
№ 7, до 18.12.05 |
6 |
|
? |
ЗАГАЛОМ: |
7 дільниць |
48 препаратів |
Переваги впровадження GMP вже реально відчувають підприємства, які мають сертифіковані виробничі дільниці. Вони значно розширили географію експорту та розпочали процедуру реєстрації українських ліків відразу у кількох країнах Східної Європи, Прибалтики, Південно-Східної Азії та Африки. В 2003 р. відповідно до рекомендацій ВООЗ було видано 151 сертифікат для міжнародної торгівлі на 32 найменування ліків у 21 країні світу. Державною службою розроблено Порядок сертифікації лікарських засобів для міжнародної торгівлі і Порядок атестації та акредитації лабораторій з контролю якості та безпеки лікарських засобів, які зареєстровано в Міністерстві юстиції (див. ).
Важливим для України є вступ Державної служби до Міжнародної конвенції національних регуляторних органів (Intrnational Conference of Drug Regulatory Authorities — ICDRA) та до системи співробітництва фармацевтичних інспекцій (PIC/S).
Невід’ємною складовою частиною системи забезпечення якості лікарських засобів є належна дистриб’юторська практика (GDP). Але досі не вжито відповідних заходів щодо впровадження цих правил та сертифікації дистриб’юторів. А це, в свою чергу, порушує цілісність системи забезпечення якості ліків під час їх обігу.
Державною службою цілеспрямовано ведеться робота щодо створення сучасної системи стандартизації фармацевтичної продукції. Наказом МОЗ затверджено низку настанов та Доповнення 1 до Державної Фармакопеї України 2001 року.
На завершення доповіді М. Пасічник коротко охарактеризував основні завдання, які стоять перед Державною службою та іншими органами державної влади.
1. Докласти всіх зусиль, щоб проект Закону України «Про внесення змін до Закону України «Про лікарські засоби» був прийнятий Верховною Радою України найближчим часом. Це буде справді рішучим кроком у напрямі подальшого розвитку фармацевтичної галузі.
2. Терміново розробити проект Закону України «Про вироби медичного призначення» для урегулювання процесів розроблення і застосування виробів медичного призначення в інтересах системи охорони здоров’я населення.
3. Розробити низку проектів постанов Кабінету Міністрів щодо вирішення проблем розвитку фармацевтичної галузі, поліпшення забезпечення населення України лікарськими засобами і виробами медичного призначення.
Крім того, необхідно вжити заходів стосовно приведення існуючих нормативних документів щодо порядку реєстрації лікарських засобів у відповідність з вимогами Указу Президента України від 7 лютого 2003 року № 91 «Про заходи щодо поліпшення забезпечення населення лікарськими засобами і виробами медичного призначення, а також підвищення ефективності державного управління у цій сфері».
У сфері інституційного забезпечення системи державного управління, регулювання та контролю обігу лікарських засобів та виробів медичного призначення в Україні потребують опрацювання питання щодо:
•?утворення територіальних органів Державної служби лікарських засобів і виробів медичного призначення, як це передбачено Положенням про неї;
•?формування в Україні мережі незалежних лабораторій з контролю якості та безпеки лікарських засобів і виробів медичного призначення;
•?оптимізації системи підготовки і перепідготовки кадрів з урахуванням необхідності запровадження правил GMP. n
Микола Холоденко, фото Євгена Чорного
* Показники імпорту та експорту наведено за групами УКТ ЗЕД 3001, 3002, 3003, 3004, 3005, 3006 «Фармацевтична продукція».
**Показники виробництва наведено на основі даних оперативної щомісячної звітності підприємств № 1-П, дані за 2003 р. будуть уточнені в травні 2004 р.



Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим