|
Традиционная тактика лечения пациентов с СД II типа предполагает постепенный переход от диетотерапии и изменения образа жизни к медикаментозной терапии. Изменение образа жизни и соблюдение низкокалорийной диеты приводит к уменьшению массы тела, что обеспечивает повышение чувствительности периферических тканей к инсулину и снижает потребность в его гиперсекреции. Таким образом, можно добиться компенсации углеводного обмена без применения медикаментозной терапии, однако сделать это удается лишь у 5–10% пациентов с впервые выявленным СД II типа в течение 1 года после установления диагноза (Недосугова Л.В., 2004). Таким образом, у тучных больных СД II типа применение лишь диеты и дозированных физических нагрузок не позволяет сохранять состояние компенсации углеводного обмена длительное время, в связи с чем рекомендуется комбинация диетотерапии с препаратами, устраняющими нарушения метаболизма. И рано или поздно при лечении таких больных врачи прибегают к медикаментозной терапии. Учитывая, что развитие СД сопровождается 2–3-кратным повышением риска кардиоваскулярной патологии, любое антидиабетическое средство следует оценивать с позиции предотвращения развития сердечно-сосудистых заболеваний и их осложнений. С этой точки зрения весьма привлекательными являются препараты из группы тиазолидиндионов, в частности — ПИОЗ.
|
Необходимо подчеркнуть, что ПИОЗ обладает доказанной биоэквивалентностью оригинальному препарату пиоглитазона. Исследования, подтверждающие это, были проведены в 2000 г. в Институте по изучению лекарственных средств, Мумбаи (Drug monitoring research institute). Это позволяет говорить о том, что ПИОЗ является по сути аналогичным оригинальному препарату пиоглитазона. |
Как уже отмечалось, наибольшее клиническое значение при СД II типа представляет потеря чувствительности к инсулину (инсулинорезистентность) мышечной, жировой и печеночной тканей. Длительно существующая инсулинорезистентность компенсируется избыточной продукцией инсулина b-клетками поджелудочной железы (гиперинсулинемией), благодаря чему поддерживается нормальный уровень углеводного обмена. Гиперинсулинемия приравнивается к маркерам инсулинорезистентности и считается предвестником развития СД II типа (Шестакова М.В., Брескина О.Ю., 2002).
Учитывая значимость инсулинорезистентности в патогенезе СД и сердечно-сосудистых осложнений, становится понятна необходимость применения для лечения пациентов с СД II типа препаратов, влияющих в первую очередь на уменьшение инсулинорезистентности. Проводимые в течение последних лет исследования по созданию таких препаратов завершились успехом, и в настоящее время в клинической практике появились лекарственные средства, объединенные по механизму их действия в группу сенситайзеров инсулина (тиазолидиндионы).
Соединения этого класса выступают в роли агонистов специфических ядерных рецепторов (PPAR-g: peroxisome proliferator-activated receptor?g) — гамма-рецепторов, активируемых пролифератором пероксисом (g-РАПП). g-РАПП обнаруживаются в ядрах клеток жировой, мышечной тканей и печени. Ядерные рецепторы семейства РАПП стимулируют транскрипцию значительного количества генов. Так, активация a-РАПП модулирует транскрипцию ряда генов, участвующих в метаболизме липидов, в частности окисления жирных кислот, в то время как g-РАПП участвуют в обеспечении адипогенеза и накоплении жирных кислот в жировой ткани. Агонисты g-РАПП, увеличивая дифференцировку адипоцитов в жировой ткани, изменяют соотношение мелких и крупных адипоцитов в сторону преобладания первых, которые, в свою очередь, проявляют более высокую чувствительность к инсулину по сравнению с крупными адипоцитами. Стимуляция g-РАПП также угнетает высвобождение провоспалительных цитокинов: фактора некроза опухоли типа альфа, интерлейкинов. Таким образом, агонисты g-РАПП — тиазолидиндионы — повышают чувствительность тканей к инсулину, что сопровождается снижением уровней глюкозы, липидов и инсулина в сыворотке крови. Иными словами, тиазолидиндионы, устраняя инсулинорезистентность, усиливают физиологическое действие собственного эндогенного инсулина и при этом снижают его концентрацию в крови. Пиоглитазон также стимулирует a-РАПП. Благодаря этому происходит активация катаболизма медиаторов воспаления, уменьшается толщина внутренней стенки артерий за счет устранения воспалительных и пролиферативных процессов, снижается уровень фибриногена в плазме крови, а также атерогенных липопротеинов (ЛП), в то время как содержание антиатерогенных (ЛПВП) — повышается. Весь комплекс изменений, происходящих в результате активации a-РАПП, приводит к замедлению прогрессирования атеросклероза (Duez H. et al., 2001).
Как и другие представители данного класса препаратов, ПИОЗ не увеличивает секрецию инсулина b–клетками поджелудочной железы. Это улучшает возможность гликемического контроля у пациентов с СД II типа при низком риске развития гипогликемии.
|
Период полувыведения пиоглитазона и его активных метаболитов составляет 16–24 ч. Поэтому пиоглитазон назначают 1 раз в день. Блистер содержит 7 таблеток ПИОЗА, которые подписаны соответственно дням недели. Это позволит пациенту помнить о приеме препарата. |
Клиническое применение пиоглитазона показало значительную его эффективность в терапии больных СД II типа. В ходе многоцентрового двойного слепого плацебо-контролируемого исследования (Aronoff S. et al., 2000), в котором принимали участие 408 пациентов, удалось показать, что применение пиоглитазона в разовой дозе 7,5; 15; 30 и 45 мг в день в качестве монотерапии сопровождалось достоверным дозозависимым снижением у больных с СД II типа уровней гликемии и гликозилированного гемоглобина (НbА1с) (рис. 1). В целом, пиоглитазон был оценен как эффективный препарат. Отмечались хорошая переносимость и отсутствие каких-либо признаков гепатотоксичности. В качестве дополнительного преимущества пиоглитазона при лечении пациентов с СД II типа, авторы отметили улучшение липидного спектра крови.
|
|
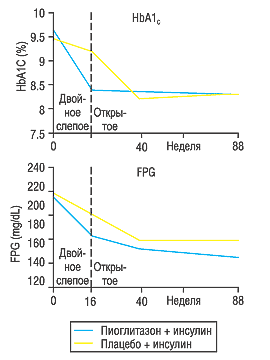
Пиоглитазон — единственный из глитазонов, разрешенный для совместного применения с инсулином. Было проведено исследование в течение 6 месяцев (Mattoo V. et al., 2005), в котором изучалось влияние комбинации пиоглитазон + инсулин на уровень гликозилированного гемоглобина (HbA1с) и содержание глюкозы в плазме крови натощак (FPG). |
Как оказалось, комбинация пиоглитазон + инсулин улучшает гликемический профиль у больных СД II типа, у которых нельзя было добиться компенсации заболевания при монотерапии инсулином (рис. 2).
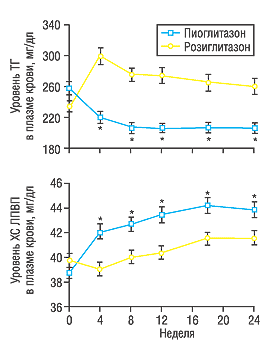
Таким образом, помимо снижения уровня гликемии, улучшение чувствительности тканей к инсулину благоприятно влияет на липидный профиль. Основное отличие пиоглитазона от других тиазолидиндионов, в частности, розиглитазона заключается в их влиянии на липидный спектр крови. В сравнительном двойном слепом рандомизированном многоцентровом плацебо-контролируемом исследовании этих двух препаратов было установлено, что пиоглитазон снижает уровень триглицеридов (ТГ) в плазме крови, в то время как розиглитазон его повышает (рис. 3). Кроме того, пиоглитазон более значительно, чем розиглитазон повышает уровень в плазме крови антиатерогенной фракции холестерина (ХС) липопротеидов высокой плотности (ЛПВП) (Goldberg R.B. et al., 2005). Нарушения липидного обмена весьма часто встречаются у больных СД, что является установленным фактором риска развития сердечно-сосудистых заболеваний. Исходя из этого, коррекция развивающейся при этом дислипидемии, прежде всего — снижение содержания в крови общего холестерина (ОХС) и липопротеидов низкой плотности (ЛПНП) и повышение антиатерогенных (ЛПВП), является одним из приоритетов как в первичной, так и во вторичной профилактике кардио-васкулярных заболеваний при СД.
|
|
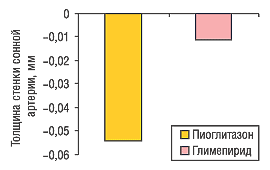
Результаты исследований также говорят о независимом антиатерогенном эффекте пиоглитазона за счет его прямого действия на сосудистую стенку (рис. 4). Как известно, толщина стенки сонных артерий является важным прогностическим маркером инфаркта миокарда и инсульта. В контролируемом рандомизированном исследовании пиоглитазон показал способность уменьшать толщину стенки сонной артерии, которая не зависела от влияния препарата на гликемический профиль плазмы крови (Langelfeld M.R. et al., 2005).
|
Проведенные исследования позволили установить новые аспекты действия пиоглитазона, что расширяет сферу применения этого препарата при терапии пациентов с СД. Так, показано, что пиоглитазон оказывает влияние на ангиогенез. Сосудистый эндотелиальный фактор роста (СЭФР, или VEGF) является ключевым регулятором внутриглазных ангиогенных заболеваний, к которым относятся диабетическая ретинопатия и возрастная дегенерация макулы. По итогам исследований отмечено, что тиазолидиндионы ингибируют интраокулярный ангиогенез (Murata T. et al., 2001). Пиоглитазон также обладает антиоксидантым эффектом (Gianinni S. et al., 2004). Кроме того, это лекарственное средство способно подавлять миграцию нейтрофилов и, следовательно, предотвращать развитие воспаления (Naito Y., Yoshikawa T., 2004).
|
Особый интерес представляет исследование PROactive, результаты которого были обнародованы на 41 съезде Европейской диабетической ассоциации. Это первое мультицентровое рандомизированное двойное слепое плацебо-контролируемое исследование, в котором приняло участие 5238 пациентов из 19 европейских стран, в ходе которого изучалось влияние пиоглитазона на развитие сердечно-сосудистых осложнений и смертность в результате них. В качестве первичных конечных точек исследователи рассматривали вероятность развития 7 разных по значимости макроваскулярных осложнений СД II типа — снижение такой вероятности произошло на 10%, однако оно не было статистически достоверным. В качестве вторичных — инфаркт миокарда, мозговой инсульт и смерть в результате них. Вероятность этих событий под влиянием пиоглитазона достоверно снизилась на 16%. Исследование подтвердило положительное влияние пиоглитазона на гликемический и липидный профиль пациентов с СД II типа, уровень АД (Charbonnel B. et al., 2005; ). |
На основании данных исследований можно сделать вывод, что пиоглитазон — действующее вещество ПИОЗА — является новым эффективным антидиабетическим средством, которое может использоваться как в качестве монотерапии, так и в сочетании с другими препаратами для лечения пациентов с СД II типа. Достоверно доказано, что применение пиоглитазона у больных с СД II типа позволяет предупредить развитие сердечно-сосудистых осложнений, особенно таких грозных как инфаркт миокарда, мозговой инсульт и смерть в результате них. o
Олег Мазуренко

 Cахарный диабет (СД) вследствие большой распространенности и крайне неблагоприятного прогноза давно находится в центре внимания ученых и врачей. В мире насчитывается около 170 млн больных диабетом, что составляет около 3% населения планеты. Особую тревогу вызывает быстрое увеличение количества больных СД. По прогнозам к 2030 г. предполагают более чем двукратное увеличение количества пациентов с СД. Ожидается, что заболеваемость СД будет увеличиваться как в развитых, так и в развивающихся странах. Выделяют два типа этого заболевания. Наибольшее внимание привлекает СД II типа (инсулиннезависимый), так как на его долю приходится около 90% всех случаев СД (WHO, 2000). Как показало исследование UKPDS, ведущей причиной смерти пациентов с диабетом II типа являются сердечно-сосудистые заболевания, прежде всего — инфаркт миокарда и острые нарушения мозгового кровообращения (Turner R.C. et al., 1998). Поражение сердечно-сосудистой системы лежит в основе 60–80% всех случаев смерти больных СД ІІ типа. Распространенность ишемической болезни сердца в данной группе больных в 2–3 раза выше, чем в общей популяции, и встречается, по некоторым оценкам, почти у 70% больных СД ІІ типа, причем у женщин чаще, чем у мужчин. При обсуждении механизмов развития сердечно-сосудистых осложнений при СД большое значение придается инсулинорезистентности и гиперинсулинемии. Инсулинорезистентность является центральным механизмом патогенеза СД II типа. Она тесно связана с сердечно-сосудистыми факторами риска, такими как АГ и дислипидемия, вносящими существенный вклад в развитие ишемической болезни сердца, поэтому для снижения риска развития осложнений необходимо не только достижение компенсации углеводного обмена, но и комплексная коррекция других метаболических нарушений. Поэтому актуальным является внедрение новых подходов в терапии пациентов с СД II типа, направленных на снижение инсулинорезистентности периферических тканей. В настоящий момент среди препаратов, способных снижать инсулинорезистентность жировой и мышечной тканей, интерес представляет ПИОЗ (пиоглитазон), производства компании «ЮСВ Лимитед» (Индия).
Cахарный диабет (СД) вследствие большой распространенности и крайне неблагоприятного прогноза давно находится в центре внимания ученых и врачей. В мире насчитывается около 170 млн больных диабетом, что составляет около 3% населения планеты. Особую тревогу вызывает быстрое увеличение количества больных СД. По прогнозам к 2030 г. предполагают более чем двукратное увеличение количества пациентов с СД. Ожидается, что заболеваемость СД будет увеличиваться как в развитых, так и в развивающихся странах. Выделяют два типа этого заболевания. Наибольшее внимание привлекает СД II типа (инсулиннезависимый), так как на его долю приходится около 90% всех случаев СД (WHO, 2000). Как показало исследование UKPDS, ведущей причиной смерти пациентов с диабетом II типа являются сердечно-сосудистые заболевания, прежде всего — инфаркт миокарда и острые нарушения мозгового кровообращения (Turner R.C. et al., 1998). Поражение сердечно-сосудистой системы лежит в основе 60–80% всех случаев смерти больных СД ІІ типа. Распространенность ишемической болезни сердца в данной группе больных в 2–3 раза выше, чем в общей популяции, и встречается, по некоторым оценкам, почти у 70% больных СД ІІ типа, причем у женщин чаще, чем у мужчин. При обсуждении механизмов развития сердечно-сосудистых осложнений при СД большое значение придается инсулинорезистентности и гиперинсулинемии. Инсулинорезистентность является центральным механизмом патогенеза СД II типа. Она тесно связана с сердечно-сосудистыми факторами риска, такими как АГ и дислипидемия, вносящими существенный вклад в развитие ишемической болезни сердца, поэтому для снижения риска развития осложнений необходимо не только достижение компенсации углеводного обмена, но и комплексная коррекция других метаболических нарушений. Поэтому актуальным является внедрение новых подходов в терапии пациентов с СД II типа, направленных на снижение инсулинорезистентности периферических тканей. В настоящий момент среди препаратов, способных снижать инсулинорезистентность жировой и мышечной тканей, интерес представляет ПИОЗ (пиоглитазон), производства компании «ЮСВ Лимитед» (Индия). 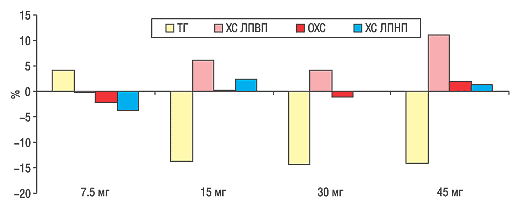
Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим