 Походження субстандартних та фальсифікованих лікарських засобів дуже різниться: від диких розвалів на просторах якихось далеких країн до діяльності цілком респектабельних європейських постачальників, які навмисно або помилково спотворюють законні ланцюжки поставок. Донедавна «під одним дахом» із зазначеними явищами перебувала і контрафактна, така, що порушує права інтелектуальної власності, продукція. Але тепер цю, природно «слизьку» категорію, віднесли до іншого кластера порушень. Які існують сучасні підходи до виявлення субстандартних та фальсифікованих лікарських засобів, та які санкції передбачені в Європі для боротьби із цим явищем?
Походження субстандартних та фальсифікованих лікарських засобів дуже різниться: від диких розвалів на просторах якихось далеких країн до діяльності цілком респектабельних європейських постачальників, які навмисно або помилково спотворюють законні ланцюжки поставок. Донедавна «під одним дахом» із зазначеними явищами перебувала і контрафактна, така, що порушує права інтелектуальної власності, продукція. Але тепер цю, природно «слизьку» категорію, віднесли до іншого кластера порушень. Які існують сучасні підходи до виявлення субстандартних та фальсифікованих лікарських засобів, та які санкції передбачені в Європі для боротьби із цим явищем?За оцінками Всесвітньої організації охорони здоров’я (ВООЗ), субстандартними або фальсифікованими є 10,5% світового обороту лікарських засобів (World Health Organization, 2017). Здебільшого цей тягар лягає на країни з низьким і середнім рівнем доходу, де, з одного боку, — багато незадоволених потреб охорони здоров’я, з іншого, — слабкість і корумпованість регуляторних та правоохоронних систем. Як зазначив нещодавно у своєму виступі д-р Тедрос Адханом Гебрейесус (Dr. Tedros Adhanom Ghebreyesus), генеральний директор ВООЗ, субстандартні та фальсифіковані ліки існують тільки через недостатню доступність якісних. «Наше головне завдання — забезпечити людям доступ до високоякісних і доступних ліків. Коли ми цього досягнемо, ринкові стимули появи неякісних та фальсифікованих лікарських засобів буде усунено», — підкреслив він.
Якщо точніше, то максимальну концентрацію даного явища ВООЗ бачить на стику 3 дефектів суспільного устрою: слабкої технічної оснащеності, обмеженої доступності ліків та незадовільного управління (рис. 1).
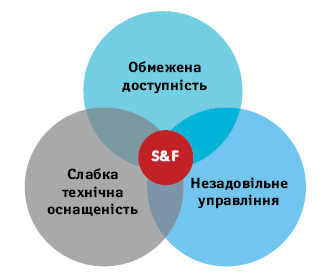
Однак перерахований набір факторів характерний для країн з невисоким рівнем доходу, тоді як у «заможних» країнах основним джерелом проблеми є складність і заплутаність ланцюжків поставок, серед яких — як повністю легальні, так і шахрайські. Однією з ілюстрацій першої є злочинна мережа, яка фігурувала в гучній справі бранденбурзького оптового оператора «Lunapharm», який постачав до Німеччини препарати, раніше вкрадені у грецьких лікарнях.
Серед відомих випадків згадують також розшифровку складного ланцюжка, кінцевими ланками якого були швейцарський паралельний імпортер, данський, британський і американський дистриб’ютори, а початковим — турецький виробник (рис. 2). Необхідність економити особисті (як у цьому випадку) або громадські (у разі «Lunapharm») кошти штовхає платників до пошуку вигідних посередників, що використовують різницю в цінах на ринках.
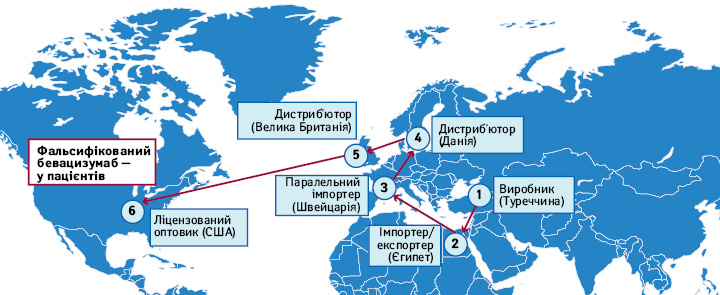
Але оскільки введення обмежень кількості задіяних постачальників не відповідає принципам вільного ринку, країни з високим рівнем доходу змушені інвестувати в удосконалення регуляторного контролю.
При цьому проста логіка підказує, що відсутність можливостей для таких інвестицій має стимулювати примусове обмеження кількості задіяних постачальників, інакше підвищення вразливості ланцюжка поставок є неминучим (рис. 3). Ще один засіб — посилення, зокрема криміналізація відповідальності за порушення в даній сфері, як, наприклад, у Ломейській ініціативі. Але слабкість владних інститутів у найбільш уражених країнах зменшує застосовність даної стратегії.
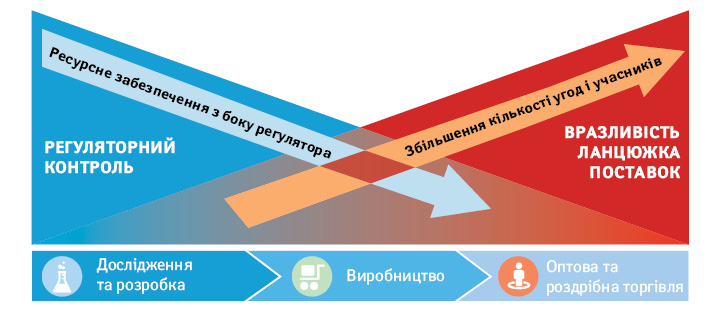
Сучасна термінологія
Рішенням ВООЗ вживаний раніше набір термінів субстандартний/підроблений/помилково маркований/фальсифікований/контрафактний (substandard/spurious/falsely-labelled/falsified/counterfeit — SSFFC) вирішено звести всього до 3 категорій: субстандартний/фальсифікований/незареєстрований (табл. 1). У відповідній заяві робочої групи відзначено, що колишня термінологія SSFFC не знаходила єдиного розуміння в міжнародному масштабі, нерідко призводячи до змішування питань якості та регуляторного схвалення з проблемами захисту інтелектуальної власності.
| Таблиця 1 | Сучасна класифікація продуктів для охорони здоров’я, яка використовується ВООЗ у глобальному нагляді й моніторингу (7th World Health Assembly, 2017) |
| Субстандартні | Незареєстровані | Фальсифіковані |
| ↑ | ↑ | ↑ |
| Також їх називають такими, що не відповідають специфікаціям: мають дозвіл на маркетинг, але не відповідають або стандартам якості, або специфікаціям, або ані тим, ані іншим | Які не пройшли оцінку та/або не отримали схвалення національними або регіональними регуляторними органами на ринку маркетування/дистрибуції або використання | Навмисно/обманним шляхом спотворюють ідентичність (суть), склад або джерело продукту |
Отже, субстандартні лікарські засоби потрапляють у законний ланцюжок розподілу і досягають пацієнтів, коли обмежена технічна можливість забезпечувати відповідність вимогам належної виробничої та дистриб’юторської практик.
Відповідно до Закону України «Про лікарські засоби» фальсифікований лікарський засіб — лікарський засіб, який умисно промаркований неідентично (невідповідно) відомостям (одній або декільком з них) про лікарський засіб з відповідною назвою, що внесені до Державного реєстру лікарських засобів України, а так само лікарський засіб, умисно підроблений у інший спосіб, і не відповідає відомостям (одній або декільком з них), у тому числі складу, про лікарський засіб з відповідною назвою, що внесені до Державного реєстру лікарських засобів України.
У цитованих матеріалах ВООЗ особливо відзначено, що визначення фальсифікованого продукту не включає ніяких аспектів, пов’язаних з правом інтелектуальної власності, оскільки для таких випадків зарезервовано термін «контрафактний». Відповідні визначення — продуктів під контрафактними торговими знаками (trademark counterfeit goods) і пов’язаних з порушенням авторських прав (pirated copyright) — можна знайти в угоді про торговельні аспекти прав на інтелектуальну власність (Trade-Related Aspects of Intellectual Property Rights — TRIPS). Продукти не мають розглядатися як фальсифіковані на тій лише підставі, що вони не мають дозволу на маркетинг у тій чи іншій країні, зазначає ВООЗ. Використовувані при цьому терміни тлумачать таким чином.
«Ідентичність» відноситься до назви, маркування, пакування або документів, що підтверджують справжність продукту, що отримав дозвіл на маркетинг.
«Склад» стосується будь-якого інгредієнта або компонента медичного продукту згідно із чинними специфікаціями, затвердженими/визнаними регулятором.
«Джерело» відноситься до ідентифікації, включаючи ім’я та адресу, власника дозволу на маркетинг, виробника, імпортера, експортера, дистриб’ютора або продавця, залежно від обставин.
Фальсифіковані продукти можуть виробляти в антисанітарних і нерегульованих умовах невідомі виробники. Кількість у них активних фармацевтичних інгредієнтів (АФІ) й ексципієнтів може бути некоректною, не виключена присутність шкідливих домішок і т.п. Упаковка фальсифікованих ліків майже завжди ідентична такій у оригінальних, тому розрізнити їх «на око» зазвичай проблематично.
Технології виявлення
Технології виявлення субстандартних та фальсифікованих ліків можна розділити на 3 великі групи:
1) візуальної ідентифікації;
2) перевірки складу продукту;
3) інформаційні.
У всіх 3 є як прості дешеві методи, так і складні дорогі. Перші 2 групи об’єднують щонайменше 4 десятки різних підходів — від контрольного списку ВООЗ (WHO Checklist) до атомно-силової мікроскопії (Kovacs S. et al., 2014). При цьому складне лабораторне обладнання (наприклад газова хроматографія) далеко не завжди є в наявності. У деяких випадках його можна замінити компактними приладами, застосування яких не потребує високого рівня підготовки (наприклад паперова хроматографія). Доступність інформаційних технологій зростає особливо високими темпами, тому вони, імовірно, найбільш універсальні (Roth L. et al., 2018). Серед них також виділяють кілька категорій (табл. 2).
| Таблиця 2 | Інформаційні засоби контролю поставок (Rasheed H. et al., 2018) |
| Категорія та тип | Призначення | Кінцевий користувач |
| Системи відстеження поставок Мобільні додатки, у тому числі ті, що розпізнають 2D-коди |
Идентифікація продукту | Аж до пацієнта |
| Бази даних (наприклад Всесвітня система нагляду і моніторингу (Global Surveillance аnd Monitoring System) ВООЗ) | Збір і аналіз інформації про фальсифіковані й субстандартні ліки | Переважно регулятори, відкритий доступ |
| Перевірка якості (тест-системи для спрощеного аналітичного контролю) | Доповнення візуальної оцінки препаратів | Уповноважені з контролю якістю на рівні торгових операторів і регулятори |
Санкції
Імплементація положень Директиви 2011/62/ЄС від 8 червня 2011 р. в законодавство країн-членів супроводжувалася зміною правових підходів щодо санкцій, пов’язаних з участю в обігу фальсифікованих та субстандартних ліків, діючих та допоміжних речовин (Report, 2018). Тепер у всіх країнах-членах щонайменше один вид відповідної діяльності тягне за собою кримінальну відповідальність (рис. 4). Причому у 21 країні це стосується виробництва, дистрибуції, посередництва, імпорту, експорту та дистанційної торгівлі. У 7 інших (Болгарія, Фінляндія, Латвія, Румунія, Польща, Швеція, Литва) до таких діянь не відносять імпорт, експорт і т.п. У названому звіті Європейської комісії можна знайти також дані про величину термінів тюремного ув’язнення і штрафів у зв’язку з тим чи іншим видом правопорушень, а також експертні оцінки їх ефективності.
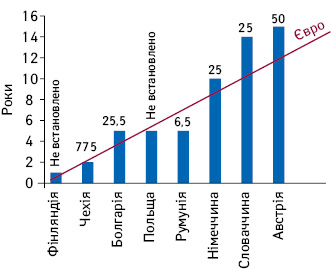
Висновок
Антифальсифікантні технології, особливо інформаційні, поряд з підвищенням обізнаності всіх зацікавлених сторін стають більш результативними в порівнянні з удосконаленням законодавства і міжнародною кооперацією як такими (Lee K.S. et al. 2017). Але «на кожну гайку знайдеться свій болт», і потрібно, щоб таких вузлів у ланцюжку поставок (угод між постачальниками), де можливим є навмисне чи випадкове спотворення ідентичності продукції, було менше. Це особливо важливо в країнах, де можливості регулятора й операторів щодо забезпечення якості залишають бажати кращого. У наступній публікації спробуємо звернутися до досвіду окремих країн ЄС у цій сфері.
Список використаної літератури
1. 7th World Health Assembly (A70/23). Provisional agenda item 13.6 from 20 March 2017 (Epub.: apps.who.int).
2. Kovacs, Stephanie & Hawes, Stephen & Maley, Stephen & Mosites, Emily & Wong, Ling & Stergachis, Andy. (2014). Technologies for Detecting Falsified and Substandard Drugs in Low and Middle-Income Countries. PloS one. 9. e90601. 10.1371/journal.pone.0090601.
3. Lee K.S., Yee S.M., Zaidi S.T.R. et al. Combating Sale of Counterfeit and Falsified Medicines Online: A Losing Battle. Front Pharmacol. 2017; 8: 268. Published 2017 May 16. doi: 10.3389/fphar.2017.00268.
4. Rasheed H., Höllein L., Holzgrabe U. Future Information Technology Tools for Fighting Substandard and Falsified Medicines in Low- and Middle-Income Countries. Front Pharmacol. 2018; 9: 995. Published 2018 Aug. 31.
5. Report from the Commission to the European Parliament and the council. Brussels, 26.1.2018 COM (2018) 49 final.
6. Roth L., Nalim A., Turesson B. et al. Global landscape assessment of screening technologies for medicine quality assurance: stakeholder perceptions and practices from ten countries. Global Health 14, 43 (2018).
7. WHO Global Surveillance and Monitoring System for substandard and falsified medical products. Geneva: World Health Organization; 2017. Licence: CC BY-NC-SA 3.0 IGO.

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим