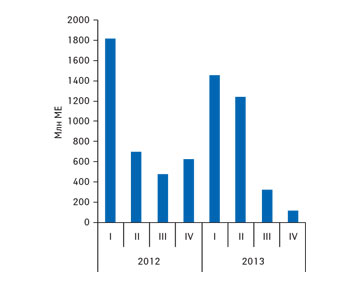
Инсулины: от госзакупок до реимбурсации
Обсуждаемые сегодня механизмы расчета предельного уровня оптово-отпускных цен позволят сократить государственные затраты на закупку препаратов инсулина с 7,0 до 10,7%
Питання доступності для населення ефективних ліків розглянуто в рамках Колегії МОЗ
В круглому столі, присвяченому цій темі, взяли участь представники профільного міністерства, Держлікслужба України, ДЕЦ МОЗ України, керівники обласних департаментів охорони здоров’я
Громадська рада при МОЗ України: діалог влади і спільноти важливий як ніколи
17 січня 2014 р. у Києві відбулося засідання Громадської ради при МОЗ України, ініційоване Міністром охорони здоров’я України
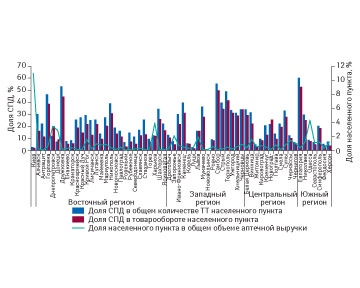
Инфраструктура аптечного рынка в разрезе форм собственности
В данной публикации мы рассмотрим инфраструктуру аптечного рынка Украины в контексте различных форм собственности как в целом по стране, так и в отдельно взятых регионах, областях и городах
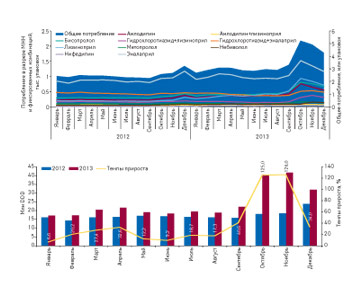
Пилотный проект – итоги 2013 г.: как изменилась структура потребления антигипертензивных препаратов
Увеличение потребления препаратов, включенных в Пилотный проект, повлекло за собой изменения в структуре потребления антигипертензивных средств в целом
Украина и тренды мирового фармацевтического рынка — интервью с главным исполнительным директором штаб-квартиры Sandoz
О том, куда движется мировой фармацевтический рынок, какие тренды развития наблюдаются сегодня, и чего стоит ожидать завтра, читайте в эксклюзивном интервью с Джеффом Джорджем
Заклади охорони здоров’я, що фінансуються з державного та місцевого бюджетів, можуть здійснювати державну закупівлю лікарських засобів, не внесених до Державного формуляру
Юридична компанія «Правовий Альянс» ініціювала звернення до МОЗ України, що було підтримано представниками фармацевтичного ринку, які стикаються з відповідною проблемою на практиці
Ліцензування імпорту лікарських засобів: зміни в законодавстві України
12 грудня 2013 р. у Києві відбувся семінар, присвячений змінам у законодавстві України у сфері ліцензування імпорту лікарських засобів та контролю за дотриманням Ліцензійних умов
Выписывание рецептов по МНН: «Все бежали, и я побежал…»
В данной публикации мы проанализируем причины введения этих регуляторных требований, целесообразность их имплементации на фармрынках различных стран, в частности в Украине, а также попытаемся ответить на вопрос — стоит ли игра свеч?
Пенсия за выслугу лет — профессиональное право фармацевтических работников
В данной публикации речь пойдет о льготных условиях пенсионного обеспечения фармацевтических работников