|
В последние годы полностью расшифрован механизм стимуляции препаратами сульфонилмочевины секреции инсулина b–клетками поджелудочной железы. Изучение молекулярных механизмов действия ПСМ позволило получить данные, проливающие свет на процессы взаимодействия различных стимуляторов секреции инсулина с рецепторами b–клеток. Секретогены инсулина, несмотря на идентичный окончательный эффект, проявляющийся в увеличении секреции и высвобождения инсулина из b–клеток, осуществляют это действие посредством вовлечения в соответствующий процесс различных белковых и сигнальных молекул. Эти препараты соединяются с рецепторами сульфонилмочевины (SUR), локализованными на мембранах b–клеток, изменяя активность К–АТФ–азы, способствуют закрытию калиевых (К–АТФ–зависимых) каналов, а это, в свою очередь, приводит к деполяризации мембраны. С другой стороны, это вызывает открытие потенциалзависимых Са2+–каналов, повышение уровня цитозольного кальция и стимуляцию Са2+–зависимого экзоцитоза секреторных гранул, в результате чего происходит высвобождение инсулина из них в межклеточную жидкость и кровь. Таким образом, мишенью действия препаратов сульфонилмочевины являются АТФ–чувствительные калиевые каналы.
У больных с СД II типа всегда имеет место более или менее выраженный дефицит инсулина, а также нарушение его секреции. В связи с этим положительный эффект применения ПСМ обусловлен их способностью стимулировать секрецию эндогенного инсулина и тем самым нивелировать его дефицит. В то же время исследователями установлено, что глипизид наряду со стимуляцией секреции инсулина обладает способностью подавлять его распад (Barzilai N. et al., 1995). Со времени внедрения ПСМ в клиническую практику не прекращаются дискуссии о внепанкреатическом (периферическом) действии этих препаратов. В течение многих лет проводятся исследования в этом направлении. Как свидетельствуют результаты экспериментальных испытаний, периферический сахароснижающий эффект глипизида обусловлен стимуляцией захвата глюкозы гепатоцитами и ускорением ее катаболизма в них, а также подавлением глюконеогенеза (Cabello M.A. et al., 1987).
Глипизид является ПСМ II поколения. Особенности химической структуры этого препарата обусловливают его большее сродство к рецепторам сульфонилмочевины на мембране b-клеток (таблица). Это означает возможность достижения терапевтического эффекта при назначении минимальных доз, на фоне которых возникновение побочных реакций практически исключено (Hu Sh. et al., 2000). В связи с этим, по сравнению с препаратами I поколения, он оказывает более выраженный сахароснижающий эффект и применяется в значительно низших дозах.
|
Таблица Сродство различных ПСМ к рецепторам b-клеток (оценка по ингибирующей концентрации – ИК50)
|
Как уже отмечалось выше, АТФ–чувствительные калиевые каналы являются первичными структурами, взаимодействующими с различными секретогенами инсулина. АТФ–чувствительные калиевые каналы представляют собой комплекс, включающий рецептор 1 к сульфонилмочевине (SUR 1) и специфический белок — так называемый внутренний очиститель калиевых каналов или ректифицирующая субъединица KIR 6.2. АТФ–чувствительные калиевые каналы построены из двух различных субъединиц — рецептора сульфонилмочевины и субъединиц калиевых каналов (KIR6.x), образующих поры и регуляторную субъединицу. Изучены три изоформы рецептора сульфонилмочевины: SUR 1 — высокоаффинный рецептор, SUR 2 и SUR 3 — низкоаффинные рецепторы. Структурно калиевые каналы в различных тканях неодинаковы по составляющим субъединицам. Так, в b–клетках островков поджелудочной железы и глюкозочувствительных нейронах гипоталамуса они состоят из SUR 1/KIR6.2; в мышце сердца — из SUR 2A/KIR6.2 и в гладкомышечных клетках сосудов — из SUR 2B/KIR6.1 (или KIR6.2). Cпособность различных препаратов (глибенкламид, глипизид, толбутамид) ингибировать калиевые каналы (SUR 1/KIR6.2 и SUR 2A/KIR6.2) значительно отличается. Так, из всех ПСМ глипизид обладает способностью в наименьшей степени ингибировать SUR 2A/KIR6.2, находящиеся в тканях сердца (Dorschner H. et al., 1999). Это может объяснить возникновение минимального количества побочных эффектов со стороны сердечно-сосудистой системы при применении глипизида. Так, исследователи в эксперименте установили, что ПСМ I поколения увеличивают, в то время как препараты II поколения уменьшают количество эктопических желудочковых сокращений и длительность транзиторных фибрилляций желудочка при перевязке левой передней венечной артерии (Ballagi-Pordany G. et al., 1990).
Развитие кардиоваскулярных осложнений у больных с СД может быть обусловлено неадекватным контролем уровня глюкозы в крови. Пик действия многих ПСМ и гипергликемия очень часто не совпадают по времени. Это приводит, с одной стороны, к недостаточному снижению уровня глюкозы в крови в течение длительного времени, а с другой — к развитию гипогликемии различной степени выраженности в последующие после приема пищи часы, особенно в случае ее недостаточного количества или пропуска приема пищи. Эпизоды гипогликемии чаще встречаются у пациентов пожилого возраста с СД II типа. Это не позволяет достичь стойкой компенсации диабета и нормализации показателей углеводного обмена как на протяжении суток, так и длительное время.

Результаты ряда исследований демонстрируют важность постпрандиальных пиков гликемии для оценки риска неблагоприятных сердечно-сосудистых исходов у больных с СД II типа. Например, исследователи выявили, что легкая и умеренная постпрандиальная гипергликемия сопровождается значительным увеличением толщины интимы и медии сонной артерии, что является начальным признаком атеросклероза (Selvin E. et al., 2005). Неблагоприятное прогностическое значение постпрандиальной гипергликемии было подтверждено в исследовании DECODE (The Diabetes Epidemiology: Collaborative Analysis of Diagnostic Criteria in Europe), в котором оценивали риск смерти при различных вариантах гипергликемии более чем у 25 000 пациентов. В этом исследовании наличие гипергликемии через 2 ч после пероральной нагрузки глюкозой сопровождалось достоверным повышением риска смерти от любых причин, в то время как гипергликемия натощак имела меньшее прогностическое значение. Эти данные свидетельствуют о том, что при оценке риска неблагоприятных сердечно-сосудистых исходов СД II типа необходимо учитывать не только уровни гликемии натощак и гликозилированного гемоглобина (HbA1c), но и содержание глюкозы в крови через 2 ч после нагрузки глюкозой (The DECODE study group, 1999).?
Таким образом, постпрандиальная гипергликемия является самостоятельным фактором риска сердечно-сосудистых осложнений СД II типа и по прогностической значимости, по крайней мере, не уступает гипергликемии натощак.
Для снижения постпрандиальной гипергликемии хорошо зарекомендовал себя глипизид, который восстанавливает первую (раннюю) фазу секреции инсулина b-клетками, имитируя естественный ритм его высвобождения. Особенностью фармакодинамики глипизида является быстрое наступление эффекта, благодаря чему это средство предупреждает повышение гликемии после еды, но не вызывает длительную гиперинсулинемию и не повышает риск гипогликемии.
Последнее крайне важное обстоятельство связано с тем, что в процессе метаболизма глипизида образуются 4 неактивных метаболита, не обладающих гипогликемическим эффектом и быстро выводящихся из организма. Абсолютная биодоступность глипизида составляет 100% ко 2–3-му часу после приема (Демидова И.Ю., 1999). Несмотря на короткий период полувыведения контроль гипергликемии достигается на протяжении как минимум 24 ч, что позволяет принимать препарат 1 раз в сутки (Shuman C.R., 1983).
ГЛИНЕЗ стимулирует секрецию инсулина в ответ на прием пищи быстро и надолго. Поэтому его основной терапевтический эффект проявляется в виде снижения постпрандиальной гипергликемии.
Эффективность глипизида в лечении пациентов с СД II типа подтверждена в? ходе нескольких двойных слепых рандомизированных исследований. В? двойном слепом плацебо-контролируемом 24-месячном исследовании у больных c СД II типа была сопоставлена эффективность монотерапии глипизидом в дозе 5 мг и метформином в дозе 500 мг. Глипизид и метформин достоверно улучшали контроль уровня глюкозы в крови, но механизм их действия был различным: глипизид снижал в основном постпрандиальную гипергликемию, в то время как метформин оказывал большее влияние на уровень глюкозы в крови натощак (Stakos D.A. et al., 2004).
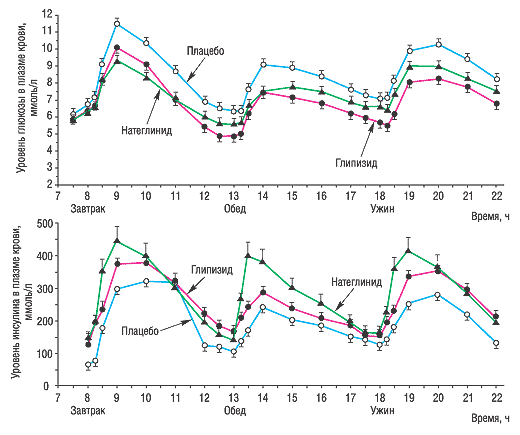
В другом двойном слепом рандомизированном плацебо-контролируемом исследовании глипизид, натеглинид, а также их комбинацию или плацебо применяли за 15–30 мин до еды. После приема пищи глипизид быстрее и эффективнее повышал уровень инсулина и уменьшал прирост гликемии после еды по сравнению с натеглинидом (Carrol M.F. et al., 2002) (рис. 1).
|
В двойном слепом рандомизированном плацебо-контролируемом исследовании изучали влияние глипизида, репаглинида и глибенкламида на постпрандиальную гипергликемию у больных c СД II типа и здоровых людей. Глипизид оказался намного эффективнее, чем глибенкламид у пациентов обоих групп, в то время как репаглинид — только у здоровых добровольцев (Cozma L.S. et al., 2002).
Во всех исследованиях переносимость глипизида была хорошей. Дозозависимых нежелательных реакций выявлено не было. Снижение уровня глюкозы в плазме крови менее 3,3 ммоль/л практически не регистрировались. На фоне комбинированной терапии частота подтвержденной гипогликемии также была низкой. Все эпизоды гипогликемии были легкими и быстро проходили.
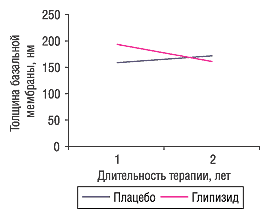
Имеются сообщения о прямом ангиопротекторном эффекте глипизида (Camerini-Davalos R.A. et al., 1988; 1994). Применение этого лекарственного средства способствует уменьшению толщины базальной мембраны капилляров, что предотвращает прогрессирование диабетических микроангиопатий (рис. 2).
|
Была доказана эффективность глипизида у пациентов с СД II типа всех возрастных групп.
ГЛИНЕЗ — прекрасно зарекомендовавшее себя средство в терапии больных с СД II типа как в начале заболевания, так и при длительном его лечении благодаря активному действию, сочетающемуся с низким риском развития гипогликемии. Особенно следует отметить, что глипизид эффективен у больных, у которых не удалось добиться нормализации гликемического профиля диетой или при применении других пероральных гипогликемизирующих средств.
Глипизид также успешно применялся для лечения пациентов с СД II типа в комбинации с инсулином. Также доказана возможность перехода с низких доз инсулина на глипизид без возникновения нарушений углеводного обмена (Shuman C.R., 1983).
В ходе 3-летнего исследования с участием 20 пациентов было установлено, что ГЛИНЕЗ нормализует уровень глюкозы в плазме крови. При этом для поддержания нормогликемии 60% пациентов было достаточно начальной дозы глипизида на протяжении всех 3 лет исследования, а 30% — даже меньшей (Mohan V. et al., 2002). Как оказалось, ГЛИНЕЗ повышает уровень С-реактивного белка в плазме крови. Ученые полагают, что благодаря такому эффекту глипизид обеспечивает защиту b-клеток поджелудочной железы. Таким образом, ГЛИНЕЗ, стимулируя высвобождение инсулина из b-клеток, не вызывает их истощения. Последнее обстоятельство особенно важно для больных с впервые установленным диагнозом СД II типа.
В контролируемых клинических исследованиях монотерапия глипизидом обеспечивала адекватный контроль нарушений углеводного обмена на протяжении 24 ч без риска возникновения постпрандиальной гипергликемии, а также периодов гипогликемии, что особенно важно для пациентов пожилого возраста.
Следовательно, ГЛИНЕЗ, действующим веществом которого является глипизид, по праву может считаться препаратом выбора в лечении впервые выявленного СД II типа и СД II типа у больных пожилого и старческого возраста, у которых уровень глюкозы в крови повышается в основном после еды и сочетается с периодами гипогликемии.?o
Олег Мазуренко

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим