|
Туберкулез — серьезная медико-биологическая и социальная проблема многих стран мира. В Европе ситуация с заболеваемостью этой инфекционной патологией носит характер пандемии, и в 2006 г. зарегистрировали 433 261 новый случай туберкулеза и 62 197 случаев смерти вследствие этого заболевания — это около 7 смертей в час. По оценкам ВОЗ в европейском регионе свыше 70% новых случаев заболевания приходится на Казахстан, Румынию, Российскую Федерацию, Турцию, Украину и Узбекистан. Ситуация практически не изменилась, а по некоторым показателям даже ухудшилась по сравнению с 2005 г., когда директор Европейского регионального бюро ВОЗ направил письмо всем государствам-членам с предупреждением о возникновении чрезвычайной ситуации в связи с распространением туберкулеза в регионе ().
Эпидемиологическая ситуация с туберкулезом в Украине остается крайне сложной. Согласно предварительным статистическим данным за 2006–2007 гг. заболеваемость всеми формами туберкулеза составила 79,8 на 100 тыс. населения (). В последние годы чаще диагностируют тяжелые деструктивные формы туберкулеза, что свидетельствует о несвоевременной, поздней диагностике по причинам, лежащим в основном вне компетенции врачей. Высокие показатели заболеваемости туберкулезом во многом являются следствием низкого экономического, образовательного и культурного уровня жизни значительной части населения, его социальной незащищенности. Распространенность туберкулеза в Украине обусловлена и процессами миграции, в том числе нелегальной, ведь, как известно, это явление сопряжено с отсутствием надлежащего диспансерного наблюдения и медицинского обслуживания (Фещенко Ю.И., Черенько С.А., 2007).
Совершенно очевидно, что фармакотерапия и профилактика туберкулеза требуют своевременного и правильного применения наиболее эффективных и безопасных ЛС.
Существуют особенности лечения туберкулеза, оказывающие существенное влияние на его результативность, среди которых особое место занимают следующие (Чуканов В.И., Каминская Г.О., Ливчане Э., 2004; приказ МЗ Украины от 09.06.2006 г.; WHO, 2003):
- длительность лечения — минимум 6 мес, 24 мес в случае химиорезистентного туберкулеза;
- комбинированное лечение — минимум 4 противотуберкулезных препарата в интенсивной фазе (2 мес) и 2 препарата в поддерживающей фазе (4 мес), для химиорезистентного туберкулеза — 5–6 препаратов в течение 6 мес в интенсивной фазе и 4 препарата в течение 18 мес в поддерживающей фазе;
- ограниченное количество противотуберкулезных ЛС: 5 противотуберкулезных ЛС I ряда для лечения новых случаев и 6 препаратов II ряда для терапии повторных случаев заболевания;
- развитие резистентности микобактерий туберкулеза к химиопрепаратам.
Проведение химиотерапии любого заболевания, в том числе и туберкулеза, к сожалению, чревато возникновением ПР, особенно при комбинированном применении ЛС, когда, к тому же, трудно выявить причинно-следственную связь между ПР и конкретным препаратом или несколькими ЛС.
Группа противотуберкулезных ЛС представлена природными и полусинтетическими соединениями, общим свойством которых является активность в отношении микобактерий туберкулеза (M. tuberculosis). Согласно общепринятой классификации противотуберкулезные ЛС делят на препараты I и II ряда:
– препараты I ряда (основные) — изониазид, рифампицин, пиразинамид, стрептомицин, этамбутол;
– препараты II ряда (резервные) — офлоксацин, ципрофлоксацин, левофлоксацин, канамицин, амикацин, капреомицин, этионамид, протионамид, тиоацетазон, пара-аминосалициловая кислота (ПАСК), циклосерин, рифабутин (приказ МЗ Украины от 09.06.2006 г.; WHO, 2003).
Такая классификация обусловлена различиями в активности и токсичности противотуберкулезных ЛС. Препараты I ряда сочетают высокую активность против M. tuberculosis и умеренную токсичность. Препараты II ряда характеризуются либо меньшей активностью, либо более высокой токсичностью, либо тем и другим одновременно. Препараты I ряда применяют для лечения пациентов с впервые выявленным туберкулезом, II ряда — при неэффективности или плохой переносимости основных противотуберкулезных ЛС (Страчунский Л.С., Козлов С.Н., 2002).
По данным Центра мониторинга ПР ЛС при ВОЗ (2007) среди противотуберкулезных монопрепаратов по частоте возникновения ПР в мире доминируют препараты изониазида — 29,2%, рифампицина — 26,7%, капреомицина — 17,1%, этамбутола — 10,2%. Менее 10% ПР были отмечены при применении пиразинамида — 9,8%, аминосалициловой кислоты — 2,2%, рифабутина — 2,1% и комбинированных ЛС.
В Украине, согласно данным Государственного фармакологического центра МЗ Украины, на противотуберкулезные ЛС приходится 2,5% всех случав ПР ЛС при медицинском применении. Следует отметить, что наиболее часто их выявляли при применении пиразинамида (монопрепарат — 33,1%), рифампицина (монопрепарат — 24,9%), изониазида (монопрепарат — 13,5%), протионамида — 6,5%, этамбутола — 5,8%, этионамида — 2,6%.
Таким образом, как в мире, так и в Украине наиболее часто ПР возникали при применении противотуберкулезных ЛС І ряда, что может быть связано с их широким использованием.
ПР противотуберкулезных ЛС развиваются в среднем у 10–15% пациентов. Примерно в 4% случаев из-за развития ПР от дальнейшего применения этих препаратов приходится отказаться. При использовании стандартных курсов химиотерапии ПР противотуберкулезных ЛС особенно часто возникают в первые 2 мес, а в последующем вероятность их развития снижается (Чуканов В.И., 2001).
ПР противотуберкулезных ЛС могут проявляться в двух формах: аллергической и токсической. Иногда разграничить такие реакции очень сложно, тогда ПР относят к токсико-аллергическим. Это разделение носит условный характер, но достаточно удобно для определения методов профилактики и лечения проявлений ПР. Отдельно выделяют дисбактериоз и его последствия.
Наиболее часто в мире сообщается о ПР аллергического генеза. Такая же ситуация характерна и для Украины. За 1996–2007 гг. среди общего количества ПР, возникших при медицинском применении противотуберкулезных ЛС, 46,4% — аллергического генеза, которые проявлялись изменениями кожи и ее производных (70,6%), аллергическими реакциями (24,4%), лихорадкой, гипертермическим синдромом (5,6%), отеком Квинке (0,2%), анафилактическим шоком (0,12%), анафилактической реакцией (0,04%). Следует подчеркнуть, что аллергологический анамнез был отягощен только у 5,8% пациентов.
Независимо от химической природы противотуберкулезных ЛС, ПР аллергического происхождения однотипны и редко возникают в течение первой недели приема препаратов, обычно — спустя 2–4 нед. Чаще всего они проявляются кожным зудом, сыпью, ринитом, повышением температуры тела, бронхоспазмом, редко — отеком Квинке, еще реже — анафилактическим шоком. Аллергические реакции редко встречаются при применении изониазида, рифампицина, этамбутола по сравнению со стрептомицином и тиоацетозоном. Однако, учитывая специфику лечения туберкулеза, определить, какое именно из назначаемых противотуберкулезных ЛС вызвало возникновение ПР, довольно сложно. Очень редко аллергические реакции развиваются одновременно ко всем препаратам стандартной схемы лечения (www.afew.org).
В табл. 1 представлены стандартные подходы к постепенному возобновлению приема противотуберкулезных ЛС после развития ПР (Харрис Э.Д., Махер Д., Грехем С., 2004).
Таблица 1
Возобновление противотуберкулезной терапии после возникновения ПР
| Препараты (в последовательности) |
Вероятность того, что препарат является причиной ПР | День 1 | День 2 | День 3 |
| Изониазид | Наименее вероятно | 50–100 мг | 300 мг | 300 мг |
| Рифампицин | ? | 75 мг | 300 мг | Полная доза |
| Пиразинамид | ? | 250 мг | 1 г | Полная доза |
| Этамбутол | ? | 100 мг | 500 мг | Полная доза |
| Стрептомицин | Наиболее вероятно | 125 мг | 500 мг | Полная доза |
По возможности во время возобновления терапии больной должен получать два противотуберкулезных ЛС, которыми он ранее не лечился. Смысл такой тактики возобновления лечения — в попытке определить, какой препарат вызвал ПР (Харрис Э.Д., Махер Д., Грехем С., 2004).
 Иногда у больных развивается гиперчувствительность к двум наиболее активным противотуберкулезным препаратам — изониазиду и рифампицину. Лечение этими ЛС является краеугольным камнем короткого курса химиотерапии. Если у больного туберкулезом без ВИЧ-инфекции развивается реакция (но не тяжелая) на изониазид или рифампицин, можно попробовать осуществить десенсибилизацию (ступенчатое наращивание дозы до полной, к примеру, за 10 дней на одну десятую каждый день). Процедура десенсибилизации весьма сложна, ее следует осуществлять только в специализированных центрах (Харрис Э. Д., Махер Д., Грехем С., 2004). В связи с вышеизложенным возникают следующие вопросы: всегда ли развитие аллергических ПР связано лишь с применением противотуберкулезных ЛС? Может ли туберкулезный процесс обусловливать возникновение аллергических реакций? На эти вопросы мы попросили ответить Светлану Черенько, доктора медицинских наук, профессора, заведующую отделением фтизиатрии Института фтизиатрии и пульмонологии им. Ф.Г. Яновского АМН Украины:
Иногда у больных развивается гиперчувствительность к двум наиболее активным противотуберкулезным препаратам — изониазиду и рифампицину. Лечение этими ЛС является краеугольным камнем короткого курса химиотерапии. Если у больного туберкулезом без ВИЧ-инфекции развивается реакция (но не тяжелая) на изониазид или рифампицин, можно попробовать осуществить десенсибилизацию (ступенчатое наращивание дозы до полной, к примеру, за 10 дней на одну десятую каждый день). Процедура десенсибилизации весьма сложна, ее следует осуществлять только в специализированных центрах (Харрис Э. Д., Махер Д., Грехем С., 2004). В связи с вышеизложенным возникают следующие вопросы: всегда ли развитие аллергических ПР связано лишь с применением противотуберкулезных ЛС? Может ли туберкулезный процесс обусловливать возникновение аллергических реакций? На эти вопросы мы попросили ответить Светлану Черенько, доктора медицинских наук, профессора, заведующую отделением фтизиатрии Института фтизиатрии и пульмонологии им. Ф.Г. Яновского АМН Украины:
|
ПР токсического генеза обусловлены избирательным влиянием противотуберкулезных ЛС на функцию различных органов и систем организма. В отличие от аллергических ПР клинические проявления токсических реакций в значительной степени зависят от дозы применяемого препарата и исходного функционального состояния органов и систем, ответственных за его метаболизм (Чуканов В.И., 2001). Наиболее часто поражаемый орган — печень, так как в ней осуществляется инактивация всех противотуберкулезных ЛС. В целом все токсические ПР этих препаратов можно разделить на нейротоксические, гепатотоксические, нефротоксические и гематотоксические.
Помимо общего токсического действия, многие противотуберкулезные ЛС обладают специфическими эффектами. Так, препараты группы аминогликозидов (стрептомицин, канамицин, амикацин, капреомицин) обусловливают поражение слухового нерва (VIII пара), этамбутол иногда ухудшает функцию зрительного анализатора, ПАСК вызывает выраженное раздражение слизистой оболочки желудка и кишечника, изолированную эозинофилию, пиразинамид — гиперурикемию и нарушение тромбоцитарного ростка кроветворения.
Кроме двух основных типов по происхождению, ПР делятся на устранимые и неустранимые (www.sitedf.ru). Устранимые ПР могут быть полностью ликвидированы или значительно ослаблены с помощью различных корригирующих средств. Они не требуют прекращения курса лечения. К неустранимым реакциям относятся клинически выраженные ПР, которые не поддаются лечебным воздействиям (потеря зрения, слуха и т.д.). При их возникновении дальнейшее применение препаратов, вызывающих эти ПР, практически невозможно.
Следует отметить, что выраженность ПР противотуберкулезных ЛС зависит от множества факторов. Особая осторожность необходима при лечении больных групп риска: люди пожилого возраста, больные с избыточной массой тела, с хроническими заболеваниями почек или печени, со склонностью к аллергическим реакциям, а также больные хроническим алкоголизмом. Многие препараты, в частности рифампицин, протионамид, стрептомицин, этамбутол и фторхинолоны, нельзя применять в период беременности из-за возможного повреждающего действия на плод, особенно в ранние сроки. Следует также учитывать способность некоторых противотуберкулезных ЛС проникать в материнское молоко, что впоследствии может привести к возникновению ПР у ребенка (Богадельникова И.В., Перельман М.И., 1997).
Одним из факторов риска, обусловливающим возникновение ПР при проведении химиотерапии, является развитие полигиповитаминоза при активном туберкулезе. При этом возникает дефицит и дисбаланс в обмене большинства витаминов группы В: В1 (тиамин), В2 (рибофлавин), В3 (пантотеновая кислота), В6 (пиридоксин) и др., а также витамина С (аскорбиновая кислота), жирорастворимых витаминов А и Е. При полихимиотерапии усугубляется исходный дефицит витамина В1, в основном за счет его биологически активной формы — тиаминдифосфата (кокарбоксилаза), а также С, Е и А — основных компонентов антиоксидантной системы (s-laboratory.narod.ru).
Далее мы остановимся на ПР, которые возникают при использовании противотуберкулезных ЛС І ряда, основные сведения об их лечении представлены в табл. 2.
Таблица 2
Oсновные тактические принципы при ПР противотуберкулезных ЛС
| ПР | Препараты | Действия врача и пациента |
| Менее серьезные | ? | Продолжать прием противотуберкулезных ЛС, проверить их дозы |
| Потеря аппетита, тошнота, боль в животе | Пиразинамид, рифампицин | Принимать ЛС с небольшим количеством пищи или перед сном |
| Боль в суставах, мышцах | Пиразинамид | Принимать ацетилсалициловую кислоту, аллопуринол |
| Повышение уровня трансаминаз | Рифампицин, изониазид, пиразинамид |
В случае, если уровень трансаминаз не нормализуется спустя месяц лечения, следует применять одновременно с ними гепатопротекторы, желчегонные средства |
| Проявления периферической нейропатии | Изониазид | Принимать пиридоксин (витамин В6), 100 мг ежедневно |
| Оранжевый/красный цвет мочи, пота, слюны | Рифампицин | Пациентов необходимо предупредить перед началом лечения, что такая ПР неизбежна, она возникает у всех пациентов и неопасна |
| Зуд, высыпания на коже | Стрептомицин, изониазид, рифампицин, пиразинамид | Приостановить применение противотуберкулезных ЛС Отменить их при значительной выраженности ПР |
| Ототоксичность | Стрептомицин | Прекратить прием стрептомицина, назначить этамбутол |
| Головокружение, нистагм, шаткая походка | Стрептомицин | Прекратить прием стрептомицина, назначить этамбутол |
| Желтуха, гепатит | Изониазид, рифампицин, пиразинамид | Отменить противотуберкулезные ЛС, контролировать уровень трансаминаз и билирубина |
| Подозрение на острую печеночную недостаточность | Большинство противотуберкулезных ЛС | Отменить противотуберкулезные ЛС, контролировать уровень трансаминаз и билирубина |
| Нарушение зрения | Этамбутол | Прекратить прием этамбутола |
| Шок, пурпура, острая почечная недостаточность | Рифампицин | Прекратить прием рифампицина |
ИЗОНИАЗИД
Применение изониазида может сопровождаться такими наиболее значимыми ПР, как нейротоксичность и гепатотоксичность, которые возникают приблизительно у 1% пациентов соответственно (www.paco.net). Также его применение может сопровождаться гематотоксическими, эндокринными нарушениями, реакциями гиперчувствительности (Рахимов К.Д., Пальгова Л.К., Аленова А.Х. и соавт., 2004).
- Нейротоксичность.
Факторы риска: пациенты — «медленные» ацетиляторы; неполноценное питание, ведущее к дефициту массы тела; период беременности, алкоголизм; сахарный диабет, эпилепсия, тяжелые психозы, уремия; заболевания нервной системы; ВИЧ-инфекция (50% больных ВИЧ/СПИДом являются больными туберкулезом, как правило, в тяжелой форме).
- Гепатотоксичность: у 10–20% пациентов проявляется временным бессимптомным повышением активности трансаминаз. В редких случаях развивается гепатит (Страчунский Л.С., Козлов С.Н., 2002).
Реже применение изониазида сопровождается возникновением следующих ПР:
- головокружение — за счет сосудорасширяющего действия изоникотиновой кислоты, образующейся в процессе ацетилирования изониазида в печени;
- реакции гиперчувствительности — лихорадка, гриппоподобный синдром, сыпь, эозинофилия, артропатия, панкреатит;
- гематотоксичность — сидеробластная пиридоксиндефицитная анемия, иногда тромбоцитопения, агранулоцитоз;
- эндокринные нарушения — гинекомастия, дисменорея, кушингоид, повышение уровня глюкозы в крови; повышение артериального давления с последующим увеличением ишемии миокарда у лиц пожилого возраста вследствие стимуляции коры надпочечников;
- тератогенность — проникая через плацентарный барьер, изониазид может вызвать миеломенингоцеле, гипоспадию, геморрагический синдром (вследствие гиповитаминоза К), задержку психомоторного развития плода.
РИФАМПИЦИН
Применение рифампицина чаще всего сопровождается развитием ПР со стороны печени (у 2% пациентов развиваются гепатотоксические реакции, у 14% пациентов наблюдают транзиторное повышение уровня трансаминаз и билирубина в сыворотке крови) (Чуканов В.И., Каминская Г.О., Ливчане Э., 2004; Gliman A.G. et al., 1990).
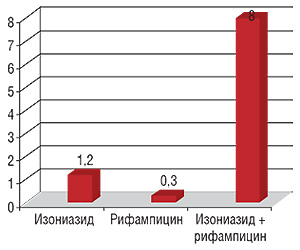
Факторы риска: алкоголизм, заболевания печени, сочетание с другими гепатотоксичными препаратами, индукторами микросомальных ферментов, в том числе изониазидом. Так, риск развития гепатита повышается у больных, принимающих одновременно изониазид и рифампицин. При этом гепатит возникает в 5–8% случаев, тогда как при монотерапии изониазидом развитие гепатита отмечают в 1,2% случаев, при монотерапии рифампицином — 0,3% (рисунок) (Чуканов В.И., 2001; ).
|
Реже при медицинском применении рифампицина возникают такие ПР:
- аллергические реакции;
- гематологические реакции: тромбоцитопеническая пурпура (иногда с кровотечением при интермиттирующей терапии); нейтропения (чаще у пациентов, получающих рифампицин в комбинации с пиразинамидом и изониазидом), гемолитическая анемия;
- гриппоподобный синдром: головная боль, лихорадка, боль в костях, артралгия, миалгия (чаще развиваются при нерегулярном приеме, при возобновлении приема препарата после перерыва в лечении);
- нефротоксичность: обратимая почечная недостаточность, чаще в ассоциации с гепатоцеллюлярными нарушениями;
- окрашивание мочи, слюны и слезной жидкости в оранжево-красный цвет (Страчунский Л.С., Козлов С.Н., 2002);
- тератогенность.
ПИРАЗИНАМИД
ПР при применении пиразинамида отмечают у 1–10% пациентов (www.umm.edu). Пиразинамид не рекомендуется назначать при тяжелых заболеваниях почек, печени, подагре, нарушениях со стороны пищеварительного тракта, гипотиреозе, эпилепсии, психозе. Выявляют такие ПР:
- диспептические явления — чаще всего тошнота и рвота;
- гепатотоксичность — тяжелые реакции при применении в обычных дозах (даже при сочетании с изониазидом и рифампицином) отмечают редко;
- нефротоксичность — интерстициальный нефрит и др.;
- гиперурикемия — отмечают у 25% пациентов, принимающих пиразинамид ();
- гематотоксичность — тромбоцитопения, сидеробластная анемия с эритроидной гиперплазией (Рахимов К.Д., Пальгова Л.К., Аленова А.Х. и соавт., 2004).
ЭТАМБУТОЛ
При применении этамбутола могут отмечать нейротоксичность. Наиболее клинически значимой потенциальной ПР является неврит зрительного нерва, который может возникнуть даже при условии назначения этого препарата в обычных терапевтических дозах.
Также применение этамбутола может сопровождаться возникновением реакций гиперчувствительности и диспептических расстройств (Рахимов К.Д., Пальгова Л.К., Аленова А.Х. и соавт., 2004).
СТРЕПТОМИЦИН
ПР при применении стрептомицина отмечают в 10–20% случаев. Наиболее часто может сопровождаться проявлением его нефротоксических и нейротоксических свойств (humbio.ru).
- Нефротоксичность: распространенность таких реакций составляет 5–25% и варьирует в зависимости от особенностей пациента, выбора препарата и режимов дозирования (), однако по сравнению с другими широко применяемыми аминогликозидами (например гентамицином) стрептомицин реже оказывает нефротоксическое действие, причем обычно развивается неолигурическая острая почечная недостаточность ().
Факторы риска: низкое артериальное давление, дегидратация, гипокалиемия, одновременное или предварительное применение петлевых диуретиков (фуросемида, кислоты этакриновой), других нефротоксических препаратов (цефалоспоринов, ванкомицина, амфотерицина В), пожилой возраст пациента, заболевания печени, печеночная недостаточность. К особо настораживающим факторам риска следует отнести заболевания почек и почечную недостаточность. Нейротоксичность: препарату свойственно ото- и вестибулотоксическое действие. Эти ПР являются следствием порой необратимых нарушений структуры и функции волосковых клеток и эфферентных волокон VIII пары черепных нервов в результате взаимодействия стрептомицина с фосфоинозитидами клеточных мембран структур внутреннего уха (Скакун М. Н., Посохова К.А., 2003; Харкевич Д.А., 2004).
 Как же повысить комплаентность больных при достаточно длительном лечении, особенно в случае развития ПР? Об этом, а также о способах повышения безопасности противотуберкулезной терапии рассказал Юрий Фещенко, доктор медицинских наук, профессор, академик АМН Украины, лауреат Государственной премии Украины в области науки и техники, лауреат премии им. Ф.Г. Яновского НАН Украины, заслуженный деятель науки и техники Украины, главный пульмонолог и фтизиатр МЗ Украины, директор Института пульмонологии и фтизиатрии им. Ф.Г. Яновского АМН Украины, заведующий отделом пульмонологии:
Как же повысить комплаентность больных при достаточно длительном лечении, особенно в случае развития ПР? Об этом, а также о способах повышения безопасности противотуберкулезной терапии рассказал Юрий Фещенко, доктор медицинских наук, профессор, академик АМН Украины, лауреат Государственной премии Украины в области науки и техники, лауреат премии им. Ф.Г. Яновского НАН Украины, заслуженный деятель науки и техники Украины, главный пульмонолог и фтизиатр МЗ Украины, директор Института пульмонологии и фтизиатрии им. Ф.Г. Яновского АМН Украины, заведующий отделом пульмонологии:
|
Ю.И. Фещенко, С.А. Черенько (Институт фтизиатрии и пульмонологии им. Ф.Г. Яновского АМН Украины), В.И. Петренко (Комитет по вопросам противодействия ВИЛ-инфекции/СПИДу и другим социально опасным заболеваниям МЗ Украины, Национальный медицинский университет им. А.А. Богомольца), В.И. Мальцев, А.П. Викторов, Е.В. Матвеева, И.А. Логвина, В.П. Яйченя (Государственный фармакологический центр МЗ Украины)
Статья публикуется в сокращенном виде

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим