 Обращение к опыту европейских стран в отношении использования ими параллельного импорта вполне может убедить в том, что инструмент этот — хороший, полезный, помогает экономить средства в бюджете здравоохранения. При этом легко забыть, что есть одно «но»: приобщиться к его ответственному применению мы не можем из-за слабости государственного управления. А вот к неадекватному — уже приобщились. Читаем свежую (опубликована 21 ноября 2019 г.) статью о параллельном импорте лекарств в Кении (Okinyi J., 2019). Проблема: фармацевтическая продукция, незаконно ввозимая в эту страну, поставляется без документов (таких как сертификаты качества и т.д.), поскольку так же нелегально осуществляют ее экспорт из стран происхождения. Последние названы в следующем порядке: Украина (!), Грузия и Турция. То есть нашими, с позволения сказать, специалистами накоплен немалый опыт в организации подобных поставок. А что, может, легализуем их в своей стране, будем получать какие-никакие налоги в казну?
Обращение к опыту европейских стран в отношении использования ими параллельного импорта вполне может убедить в том, что инструмент этот — хороший, полезный, помогает экономить средства в бюджете здравоохранения. При этом легко забыть, что есть одно «но»: приобщиться к его ответственному применению мы не можем из-за слабости государственного управления. А вот к неадекватному — уже приобщились. Читаем свежую (опубликована 21 ноября 2019 г.) статью о параллельном импорте лекарств в Кении (Okinyi J., 2019). Проблема: фармацевтическая продукция, незаконно ввозимая в эту страну, поставляется без документов (таких как сертификаты качества и т.д.), поскольку так же нелегально осуществляют ее экспорт из стран происхождения. Последние названы в следующем порядке: Украина (!), Грузия и Турция. То есть нашими, с позволения сказать, специалистами накоплен немалый опыт в организации подобных поставок. А что, может, легализуем их в своей стране, будем получать какие-никакие налоги в казну?И картели сыты, и аптеки целы…
Кения стала второй из африканских стран, принявших законодательство, разрешающее параллельный импорт недорогих антиретровирусных препаратов (Siringi S., 2001). Законопроект о промышленной собственности, принятый парламентом 12 июня 2001 г., разрешил параллельный импорт оригинальных лекарственных средств из государств, где они продаются по более низкой цене.
По данным Кенийской ассоциации фармацевтической промышленности (Kenya Association of Pharmaceutical Industry), генерики (непатентованные лекарственные средства) не подлежат параллельному импорту, поскольку правительство может обеспечивать ими с помощью более легких способов (www.kapikenya.org).
Надо ли говорить, что цели нововведения декларировали весьма благие: «В результате реализации этой политики на местном фармацевтическом рынке будут ликвидированы картели, что принесет пользу населению. Монополии были проблемой в этой отрасли, потому что они предоставляли возможность для ввоза некачественных лекарственных средств и подделок на кенийский рынок, — отмечал профильный специалист из местного регуляторного органа Энтони Торойтич (Antony Toroitich). — Они (картели) повысили стоимость лечения, манипулируя динамикой спроса и предложения, что порождает дефицит основных лекарственных средств и в конечном итоге повышает их цену; делают они это ради собственной эгоистичной выгоды».
И что же, получили бедные кенийцы доступ к дешевым лекарственным средствам из-за рубежа? Нет, конечно! Цитата из вышеназванной свежей статьи: «Параллельные импортеры также утверждают, что цена, которую они предлагают, намного ниже по сравнению с авторизованными импортерами/дистрибьюторами. В некоторых случаях это может быть правдой, однако такая экономия редко бывает действительной для пациента, так как розничный продавец, который непосредственно отпускает лекарства, обычно максимизирует свою прибыль за счет огромной разницы между закупочной и отпускной ценами…
Это наблюдалось в некоторых ведущих больницах в Найроби, которые покупают параллельное импортное лекарственное средство и продают по ценам, таким же или даже более высоким, чем у авторизованного импортера. Препараты идут в основном на нужды застрахованных пациентов».
«Мерками, ведрами, горшками!»
«Вriefcase traders» (портфельные торговцы) — таким деликатным оборотом обозначает кенийский автор нелегальных импортеров фармацевтической продукции в свою страну, просто в английском языке нет подходящего слова для обозначения грязных баулов, в которых «челноки» таскают свой товар через границу. Хотя почему баулы? Наверняка, объемы там вполне промышленные.
В остальном автор вполне «в теме»: называет «пропускные пункты», через которые кенийские дельцы доставляют продукцию из соседней Уганды, или самолетами (теми же бортами, что перевозят в Могадишо местную «травку» — листья ката) — из Сомали. Таможенные чиновники, сотрудники транспортных, логистических операторов — все повязаны между собой в данном незаконном бизнесе.
У розничных операторов — также своя сеть доверенных представителей с выходом на лечебные учреждения. Такое подробное описание приведено здесь для того, чтобы незнакомым с проблемой читателям не казалось, что имеет место некий заговор по очернению (?) Украины заодно с Кенией.
А что они поставляют?
Да, в общем, в Китае и Индии все есть, может, и в Украине тоже. Во всяком случае, по оценкам Всемирной организации здравоохранения (ВОЗ), субстандартными или фальсифицированными являются 10,5% мирового оборота лекарственных средств (World Health Organization, 2017). По большей части это бремя ложится на страны с низким и средним уровнем дохода (Bulletin of the World Health Organization, 2010).
Субстандартные лекарственные средства официально определяют как получившие разрешение на маркетинг, и при этом не соответствующие стандартам качества и/или спецификациям, что может быть связано с недостатками производства, доставки или хранения, или пребыванием в обращении после истечения срока годности. Фальсифицированные — как намеренно/мошеннически искажающие свою идентичность, состав или происхождение (World Health Organization, 2017 а).
Среди 96 исследований, в которых оценивалась распространенность некачественных основных лекарственных средств в странах с низким и средним уровнем дохода (с проверкой 50 или более образцов в каждом исследовании), при общей выборке, составившей 67 839 препаратов, общая распространенность некачественных составила 13,6% (95% доверительный интервал (ДИ): 11,0–16,3%), а региональная распространенность — 18,7% — в Африке (95% ДИ: 12,9–24,5%) и 13,7% — в Азии (95% ДИ: 8,2–19,1%) (Ozawa S. et al., 2018).
Из исследований, включенных в метаанализ, 19,1% (95% ДИ: 15,0–23,3%) противомалярийных препаратов и 12,4% (95% ДИ: 7,1–17,7%) антибиотиков были некачественными или фальсифицированными. При этом 8 оценок глобальных экономических последствий дали значения в диапазоне 10–200 млрд дол. США (медиана — 31,25 млрд дол.).
Великобритания
В странах со «строгими регуляторными системами» у регуляторов — много работы, ныне они внедряют официальные программы для отслеживания нарушений и управления ими в режиме онлайн. В 2017/2018 отчетном году Агентством по контролю за лекарственными средствами и медицинскими изделиями Великобритании (Medicines and Healthcare products Regulatory Agency — MHRA) были инициированы процессы с обвинительными заключениями в отношении 10 обвиняемых и получены постановления о конфискации на сумму 2 млн фунтов стерлингов (Gilbert K., Lodge G., 2019).
Правоприменение в подобных случаях осуществляют преимущественно путем уголовного преследования. Однако владельцы товарных знаков могут также инициировать гражданское разбирательство в связи с нарушением своих прав.
Соединенное Королевство является одной из 123 стран, участвующих в операции «Pangea», цель которой — препятствование реализации контрафактных и незаконных лекарственных средств и медицинских изделий через интернет. В 2017/2018 отчетном году это привело к изъятию 1,3 млн упаковок фальсифицированных и нелицензированных препаратов с оценочной стоимостью 4,1 млн фунтов стерлингов и закрытию 3500 веб-сайтов в Соединенном Королевстве.
Швейцария
По поручению Швейцарского агентства по лекарственным средствам (Swissmedic) Швейцарская таможня изъяла 1028 (партий?) нелегально ввезенных лекарственных средств в 2016 г. (1134 — в 2015 г.). Из них 48% родом из Индии (42% в 2015 г.) и 21% (18% в 2015 г.) — Западной Европы (особенно Великобритании, Германии и Португалии), а 13% (24% в 2015 г.) — из других азиатских стран (Flury R., 2018).
Около 55% этих препаратов — предназначенные для лечения эректильной дисфункции, а 13,5% — снотворные и транквилизаторы. Незаконный ввоз лекарственных средств карается уголовными санкциями и может повлечь за собой значительные штрафы, в том числе для физических лиц. При этом не раз сообщали о неудовлетворительном качестве нелегально ввозимых препаратов.
Для параллельного импорта лекарственных средств требуется разрешение Swissmedic, которое можно получить в упрощенном порядке. В случае лекарственных средств, цены на которые регулируются правительством и которые все еще защищены патентами, параллельный импорт разрешается только с согласия владельца патентов.
Поскольку упаковка лекарственных средств выполняет важную функцию, любое ее изменение (например удаление или сокрытие какой-либо информации) представляет собой нарушение прав владельца на товарный знак. Несмотря на это, владелец не может запрещать переупаковку препаратов, если таковая необходима для отпуска поступающих путем параллельного импорта.
Сложности добавляет то, что в соответствии со швейцарскими правилами маркировка и инструкции должны быть переведены на три официальных языка (немецкий, французский и итальянский). Дополнительное требование для получения разрешения от Swissmedic (даже если его можно получить с помощью упрощенной процедуры) означает, что на практике в Швейцарии практически отсутствует параллельный импорт лекарственных средств. Следовательно, проблемы, связанные с переупаковкой, возникают редко.
Германия
Отраслевые ассоциации призывают законодателя к введению запрета на параллельное распространение лекарственных средств. Причина: каналы распределения и цепочки поставок лекарств в Европейском Союзе и за его пределами слишком запутаны и часто приводят в последние годы к криминальным манипуляциям или провоцируют их. «Параллельное распространение лекарственных препаратов все чаще используется в качестве канала незаконного сбыта, в том числе поддельных лекарственных средств. Недавний пример — так называемый скандал с «Lunapharm», — отмечено в заявлении.
Так, по информации, представленной на сайте министерства здравоохранения Германии, бранденбургский оптовый оператор «Lunapharm» получил в греческой аптеке дорогостоящие лекарства от рака. Препараты, ранее украденные в греческих больницах, продавали в Германии через аптеки, оптовых операторов и прочих импортеров.
Достоинства и недостатки параллельного импорта
Аргументы «за»:
1. Прямое снижение цен на оригинальные лекарственные средства.
2. Косвенное снижение — дополнительный аргумент в переговорах с производителями оригинальных препаратов.
Аргументы «против» (по Peiravian F., 2014; www.iracm.com):
1. Интеграция рынков посредством параллельного импорта может приводить к повышению цен в странах-экспортерах за счет сокращения объема продукции, остающейся в местной цепочке обращения. Производители могут пренебрегать данными рынками.
2. Затраты на транспортировку и переупаковку в параллельной торговле могут уменьшить значительную долю любых потенциальных ценовых преимуществ.
3. Параллельные дистрибьюторы не несут затрат на исследования и разработки (R&D), а также маркетинг. Обычно они пользуются маркетинговыми усилиями оригинальных производителей и их партнеров, которые по этой причине могут посчитать невыгодным продолжение подобной деятельности на рынках-экспортерах.
4. Параллельный импорт снижает рентабельность производителей оригинальных препаратов. Это может повлиять на их программы R&D, которые чувствительны к такому сокращению прибыли, и может привести к замедлению глобальной разработки лекарственных средств.
5. Искусственное умножение количества посредников. В отличие от традиционной схемы распределения (производитель лекарственных средств/оптовик/аптека), параллельный импорт приводит к появлению новых, а иногда и очень многочисленных игроков (покупателей, «переупаковывающих» агентов, перевозчиков и т.д.). Это угрожает безопасности распределительной цепочки, повышает риск фальсификаций, затрудняет контроль.
6. Систематическая переупаковка лекарственных средств. В случае препарата, импортируемого параллельно, продукт должен быть переупакован для приведения его в соответствие с национальным законодательством страны-импортера, особенно в отношении языка. Такие операции по переупаковке могут ограничиваться наклеиванием дополнительных этикеток на оригинальную упаковку и вставкой инструкций на языке страны импорта; возможно также полное изменение упаковки и создание новой. Отсюда — путаница или ошибки в инструкциях и упаковке, дополнительные трудности с отзывом партий, несоблюдение условий хранения и т.д.
В отсутствие согласованных систем между странами-импортерами и экспортерами это подрывает прослеживаемость препарата. Например, некоторые параллельные импортеры перенумеровывают партии во время операций по переупаковке. Это обусловливает наличие разных номеров на первичной и вторичной упаковках.
Кроме того, для удовлетворения требований некоторых стран по согласованию количества единиц в упаковке с таковой у получившего разрешение на маркетинг местного продукта некоторые импортеры иногда срезают блистеры, чтобы уменьшить в них количество таблеток или капсул.
Наконец, что станет с оригинальной упаковкой лекарств? Будут ли ее систематически уничтожать для гарантии, что недобросовестный производитель не использует ее повторно? При отсутствии таких гарантий переупаковка может облегчить работу недобросовестных операторов.
7. Из-за отсутствия достаточного контроля за маршрутом транспортировки лекарственных средств при параллельной торговле (например тех, которые нуждаются в соблюдении условий холодовой цепи) может быть нарушено качество препаратов. Поскольку владельцы торговых марок не несут ответственности за подобные нарушения, вопросы ответственности не имеют однозначных решений.
8. Создаются повышенные требования к мощности лабораторий для выявления некачественных и контрафактных препаратов.
9. Неоднозначна надежность поставок лекарственных средств, задействованных в параллельном распределении.
Альтернативы
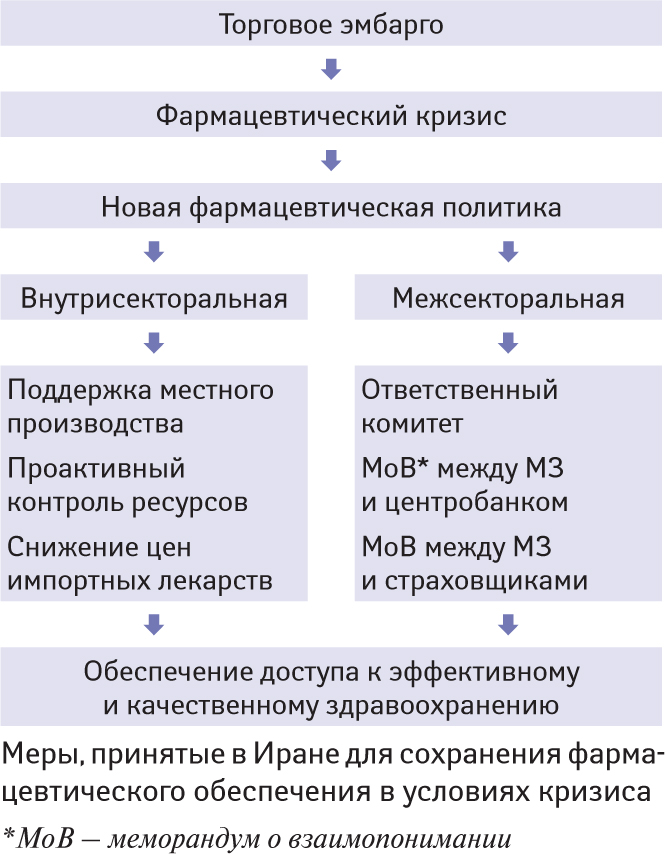
Похоже, чрезмерная открытость вредит странам с «нестрогой» регуляторной системой и неустоявшимися рыночными отношениями. Как это ни парадоксально, но хорошим примером стратегий устойчивости в подобных ситуациях является опыт, благодаря которому иранский фармацевтический сектор выстоял во время международных санкций. Стратегия выживания предусматривала, в частности (Yousefi N., 2019):
- значительное снижение цен импортируемых лекарств и сокращение их рыночной доли;
- содействие местному производству лекарств с привлечением иностранных инвестиций;
- оказание финансовой поддержки всем пациентам (рисунок).
Универсальными стратегиями являются также:
- переговоры с поставщиками и владельцами торговых марок с целью снижения стоимости их лекарств;
- разработка клинически обоснованных и не зависящих от рыночной конъюнктуры формуляров и протоколов лечения с опорой на взаимозаменяемость (в том числе среди препаратов me-too) и многоисточниковость.
Однако никакие позитивные сдвиги в фармацевтической политике невозможны без наличия государственной воли, действующей в интересах населения и системы здравоохранения страны.
Дарья Полякова
Список использованной литературы
- 1. Flury R. (2018) Procedures and strategies for pharmaceutical brands: Switzerland. Epub.: www.worldtrademarkreview.com.
- 2. Gilbert K., Lodge G. (2019) Procedures and strategies for pharmaceutical brands: United Kingdom. Epub.: www.worldtrademarkreview.com.
- 3. Growing threat from counterfeit medicines (2010) Bull World Health Organ., Apr; 88(4): 247–8.
- 4. Okinyi J. (2019) Why the govt must curb parallel importation of medicines. Epub.: www.capitalfm.co.ke/eblog/why-the-govt-must-curb-parallel-importation-of-medicines.
- 5. Ozawa S., Evans D.R., Bessias S. et al. (2018) Prevalence and Estimated Economic Burden of Substandard and Falsified Medicines in Low- and Middle-Income Countries: A Systematic Review and Meta-analysis. JAMA Netw. Open.; 1(4): e181662. Published 2018 Aug 3. doi: 10.1001/jamanetworkopen.2018.1662.
- 6. Peiravian F. (2014) Parallel import: is it worth?. Iran J. Pharm. Res.; 13(4): 1111–1114.
- 7. Siringi S. (2001) Kenya allows parallel importation of drugs. The Lancet, vol. 357, issue 9273: 2034.
- 8. Toroitich A. (2017) Parallel importation of drugs to lower cost of medication. Epub.: pharmacyboardkenya.org/blog/2017/12/parallel-importation-of-drugs-to-lower-cost-of-medication.
- 9. World Health Organization (2017) A Study on the Public Health and Socioeconomic Impact of Substandard and Falsified Medical Products. Geneva, Switzerland: World Health Organization.
- 10. World Health Organization (2017а) Seventieth World Health Assembly Update, 29 May. Geneva, Switzerland: World Health Organization.
- 11. Yousefi N., Moradi N., Dinarvand R. et al. (2019) DARU J. Pharm. Sci. 27: 169.

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим