3. НОВЫЕ ПРОЦЕДУРЫ ПО ПЕРЕСМОТРУ И РАСПРОСТРАНЕНИЮ ПРИМЕРНОГО ПЕРЕЧНЯ ОЛС (ПРОДОЛЖЕНИЕ)
3.4 Примерный формуляр ВОЗ
На заседании, состоявшемся в 1995 г., Комитет экспертов ВОЗ по отбору и использованию основных лекарственных средств (ОЛС) рекомендовал ВОЗ разработать примерный формуляр в дополнение к Примерному перечню ОЛС, который стал бы подспорьем для стран, стремящихся к созданию собственных национальных формуляров (The use of essential drugs. Seventh report of the WHO Expert Committee. Geneva, World Health Organization, 1997 — WHO Technical Report Series, № 867). Предусматривалось, что пересмотр такого примерного формуляра должен осуществляться каждые 2 года.
На нынешнем заседании Комитет сообщил о ходе разработки Типового формуляра ВОЗ (WHO model formulary). После проведения ряда консультаций (в 1996, 1997 и 1999 г.) к концу 1999 г. был готов первый проект Типового формуляра. В начале 2000 г. была достигнута договоренность о том, что Королевское фармацевтическое общество Великобритании (которое в сотрудничестве с Британской медицинской ассоциацией опубликовало Британский национальный формуляр) возьмет на себя ответственность за проверку и окончательную доработку первой редакции Типового формуляра ВОЗ.
В ходе редакционного процесса все положения предварительного текста были сопоставлены с оригинальными источниками, приведены в соответствие с другими документами и рекомендациями ВОЗ, а также авторитетными источниками сведений о ЛС, в том числе публикуемой регуляторной информацией.
Изменения, которые вносились в предварительный текст в ходе проведения проверок достоверности данных, обоснование этих изменений и соответствующие ссылки опубликованы. При необходимости в текст вносились изменения с учетом новых данных, которые были опубликованы после подготовки основного предварительного текста. Кроме того, к предварительному тексту прилагались монографии, касающиеся некоторых ОЛС, включенных в Примерный перечень ВОЗ на заседании Комитета, состоявшемся в ноябре 1999 г. (The use of essential drugs. Ninth report of the WHO Expert Committee (including the revised Model List of Essential Drugs). Geneva, World Health Organization, 2000 — WHO Technical Report Series, № 895).
Первоначально предполагалось сохранить структуру разделов и систему нумерации Примерного перечня ОЛС ВОЗ, но осуществить это на практике оказалось трудно, в основном потому, что в Примерном перечне разделы не всегда совпадают с терапевтическими категориями и не всегда согласуются с вводными оценочными формулировками. В этой связи были произведены некоторые изменения, в результате которых в разных разделах Примерного формуляра ВОЗ повторяются статьи о препаратах, относящихся к нескольким (более одной) терапевтическим категориям. Неполное соответствие нумерационной системе Примерного перечня не представляется серьезной проблемой. Пользователи Типового формуляра ВОЗ могут найти интересующие их сведения с помощью оглавления или основных индексов (включают как наименования ЛС, так и нозологические формы).
Текст Типового формуляра ВОЗ должен быть доступен в различных электронных форматах, в том числе на CD-ROM, в Интернете на веб-сайте Библиотеки ВОЗ по ОЛС, и снабжен гиперссылками на Примерный перечень ОЛС ВОЗ. Электронная версия Типового формуляра ВОЗ может служить своеобразным практическим пособием для стран, стремящихся разработать собственные формуляры. Национальные или учрежденческие комитеты по составлению формуляров могут использовать Типовой формуляр ВОЗ исходя из собственных первоочередных задач: изменяя содержащиеся в нем положения, приводя в соответствие с ним национальные формуляры путем добавления в них новых или исключения существующих препаратов.
Когда состоялось заседание (апрель 2002 г.), первая редакция Типового формуляра ВОЗ находилась на финальной стадии редакционного процесса; электронную версию документа планировалось сделать доступной для пользователей до конца 2002 г. (WHO model formulary 2002. Geneva, World Health Organization, 2002). Комитет экспертов ВОЗ подчеркнул, что первый проект текста Типового формуляра ВОЗ разработан на основе 10-го Примерного перечня ОЛС ВОЗ (пересмотра 1997 г.), в настоящее время он приведен в соответствие с 11-м Примерным перечнем (пересмотра 1999 г.). Комитет экспертов ВОЗ рекомендовал до опубликования окончательного варианта еще раз пересмотреть Типовой формуляр и отразить в нем изменения, которые будут внесены в Примерный перечень в ходе нынешнего заседания.
В соответствии с запросом секретариата ВОЗ Комитет также рекомендовал пересмотреть Приложение 3 к Типовому формуляру ВОЗ, касающееся применения ЛС в период кормления грудью, поскольку данное Приложение составлено на основе устаревшей публикации ВОЗ 1995 г. «Кормление грудью и медикаментозное лечение матери» (Breastfeeding and maternal medication. Geneva, World Health Organization, 1995. WHO/CDR/95.11).
Пересмотреть представленный текст Типового формуляра с учетом препаратов, заявки о внесении которых в Примерный перечень ОЛС ВОЗ представлены для рассмотрения на данном заседании Комитета экспертов ВОЗ (согласно новым процедурам), не представляется возможным в связи с недостатком времени. При этом Комитет признал важное значение Типового формуляра ВОЗ для составления и использования Примерного перечня ВОЗ и необходимость рассмотрения обоих документов в странах, в которых ведется разработка национальных перечней ОЛС.
3.5. Библиотека ВОЗ по ОЛС
В 1975 г. Всемирная ассамблея здравоохранения (World Health Assembly — WHA) обратилась в ВОЗ с просьбой предоставить сведения о качестве, ценовых и терапевтических особенностях отдельных препаратов, входящих в Примерный перечень ОЛС ВОЗ. На предыдущем заседании (в 1999 г.) Комитет экспертов ВОЗ указал на важность установления связи между отбором ОЛС для Примерного перечня, Типовым формуляром и клиническими рекомендациями ВОЗ (The use of essential drugs Ninth report of the WHO Expert Committee (including the revised Model List of Essential Drugs). Geneva, World Health Organization, 2000; WHO Technical Report Series, № 895). Тогда же Комитет поддержал предложение о более широком освещении доказательных данных, которыми Комитет оперирует в ходе работы, и рекомендовал тщательно фиксировать доводы, на основании которых принимаются окончательные рекомендации о внесении препаратов в Примерный перечень ОЛС ВОЗ или об их исключении.
Новые процедуры по пересмотру и распространению Примерного перечня ОЛС ВОЗ включают создание Организацией электронной Библиотеки по ОЛС с целью сделать более доступной информацию об ОЛС с помощью CD-ROM и Интернета (см. раздел 3.2.). В структуре Библиотеки предусмотрены ссылки на клинические рекомендации ВОЗ, Типовой формуляр ВОЗ и международные справочные руководства по ценам на ЛС, представлены международная лекарственная номенклатура и стандарты качества препаратов.
Комитет экспертов был проинформирован о процессе создания Библиотеки по ОЛС. На момент заседания была создана структура базы данных с включением в нее Примерного перечня ОЛС ВОЗ, краткого обоснования в пользу включения в Примерный перечень каждого из препаратов и ссылок на систематические научные обзоры. Подготовка резюме клинических рекомендаций ВОЗ находится на завершающей стадии, гиперссылки на Типовой формуляр ВОЗ — в процессе разработки. Комитет определил цель: открыть веб-сайт Библиотеки по ОЛС до конца 2002 г., после чего добавлять недостающие элементы Библиотеки по мере их подготовки. Схема структуры Библиотеки ВОЗ по ОЛС и ее основных «внешних» взаимосвязей представлена на рисунке.
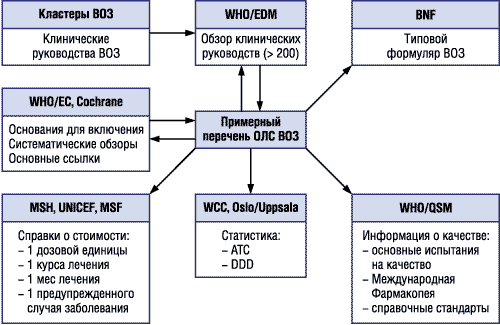 |
ATC — Анатомотерапевтическая и химическая классификационная система ЛС (Anatomical Therapeutic Chemical classification — АТС); BNF — Британский национальный формуляр; Cochrane — Кокрановское сотрудничество (Cochrane Collaboration); DDD — установленные суточные дозы; MSH — организация «Науки управления для здравоохранения» (Management Sciences for Health); MSF — организация «Врачи без границ» (Medecins sans Frontieres); UNICEF?— ЮНИСЕФ; WHO/EC — Комитет экспертов ВОЗ по отбору и использованию ОЛС; WHO/EDM — Департамент ОЛС, ВОЗ; WCC — Центр Сотрудничества ВОЗ (WHO Collaborating Centre) в г. Осло и г. Уппсала; WHO/QSM — Группа по обеспечению качества и безопасности ЛС (Департамент ОЛС, ВОЗ).
Рисунок. Структура Библиотеки ВОЗ по ОЛС
Комитет экспертов высказал удовлетворение достигнутыми результатами и признал необходимость использования в рамках деятельности Библиотеки ВОЗ по ОЛС всех доступных средств распространения информации начиная с пересылки электронной информации в национальные центры с помощью CD-ROM и интернета и заканчивая распространением на местах. Кроме того, по запросу, направленному в Департамент ВОЗ по ОЛС и лекарственной политике, могут предоставляться специальные электронные файлы (запросы на получение информации следует направлять по адресу: Department of Essential Drugs and Medicines Policy, World Health Organization, 1211 Geneva 27, Switzerland).
Что касается содержания Библиотеки ВОЗ по ОЛС, то Комитет экспертов рекомендовал разместить на соответствующем веб-сайте подробную информацию о заявках на внесение в Примерный перечень всех новых препаратов (с обоснованием целесообразности внесения), протоколы с решением Комитета экспертов, а также заархивированные данные о повестке дня предыдущих заседаний.
Комитет экспертов ВОЗ отметил, что информация, представленная «под зонтиком» Библиотеки ВОЗ по ОЛС, поддерживается в основном за счет внешних информационных источников, которые не входят в сферу ее контроля и ответственности. Исключение составляют фрагменты Типового формуляра ВОЗ, посвященные новым препаратам, внесенным в Примерный перечень ОЛС ВОЗ. Хотя Типовой формуляр не получил официального одобрения Комитета экспертов ВОЗ, он был разработан согласно рекомендациям Комитета. Более того, Типовой формуляр является полным банком информации, которую Комитет стремится сделать доступной при разработке своих рекомендаций относительно внесения препаратов в Примерный перечень ОЛС ВОЗ. В этой связи Комитет одобрил содержащееся в новых процедурах требование, в соответствии с которым текст Типового формуляра ВОЗ о новом препарате должен рассматриваться Комитетом одновременно с заявкой о включении данного препарата в Примерный перечень.
Согласно рекомендациям Комитета ключевые разделы Библиотеки ВОЗ по ОЛС должны быть доступны не только на английском, но и на других языках. Для этого ВОЗ рекомендует рассмотреть возможность и потенциальные преимущества разработки гиперссылок на соответствующие иноязычные веб-сайты и веб-сайты, учрежденные органами по регулированию ЛС. В систематических обзорах о препаратах, предложенных для включения в Примерный перечень, могут быть рассмотрены статьи, опубликованные в независимых изданиях.
4. ДРУГИЕ ВАЖНЫЕ ТЕХНИЧЕСКИЕ ВОПРОСЫ
4.1. Изменение названия Комитета экспертов ВОЗ
Созванный в 1977 г. первый Комитет экспертов ВОЗ получил название «Комитет экспертов ВОЗ по отбору основных лекарственных средств» (WHO Expert Committee on the Selection of Essential Drugs), а отчет о его заседании — The selection of essential drugs Report of a WHO Expert Committee. Geneva, World Health Organization, 1977 (WHO Technical Report Series, № 615). Эти названия были оставлены Комитетом без изменений на его втором заседании в 1979 г.: The selection of essential drugs. Second report of a WHO Expert Committee. Geneva, World Health Organization, 1979 (WHO Technical Report Series, № 641). На третьем заседании в 1982 г. Комитет был переименован в «Комитет экспертов ВОЗ по использованию основных лекарственных средств» (WHO Expert Committee on the Use of Essential Drugs), а отчет о его заседании — The use of essential drugs. Report of a WHO Expert Committee Geneva, World Health Organization, 1983 (WHO Technical Report Series, № 685).
В ходе разработки на протяжении 2001 г. новых процедур по пересмотру и распространению Примерного перечня ОЛС ВОЗ (см. раздел 3.1; «Еженедельник АПТЕКА», № 28 (399) от 28 июля 2003 г. — Прим. переводчика), ВОЗ стала использовать термин «essential medicines» как альтернативу «essential drugs». Среди причин изменения терминологии следует отметить следующее:
• Термин «medicines» является общепринятым для обозначения ЛС, используемых в практическом здравоохранении.
• Для людей, для которых английский язык не является родным, слово «drugs» часто ассоциируется с наркотическими или запрещенными веществами (сильнодействующими наркотиками). Поэтому не всегда понятно, что подразумевается под словосочетанием «national drug policy» (национальная лекарственная политика).
• Для других языков, например французского и испанского, двойное значение не характерно: «mўеdicaments essentials» и «medicamentos esencialоs» являются общепринятыми официальными терминами.
• 2002 г. знаменателен не только в связи с 25-й годовщиной со дня принятия Примерного перечня ОЛС ВОЗ, но и в связи с учреждением Библиотеки ВОЗ по ОЛС; совпадение этих двух важных событий — подходящий повод для «перемены имен».
Основной целью нынешнего заседания Комитета экспертов ВОЗ является разработка рекомендаций по отбору ОЛС. В то же время отбор ЛС нельзя рассматривать в отрыве от их использования, что подтверждается увеличением удельного веса стандартных клинических рекомендаций и созданием Библиотеки ВОЗ по ОЛС. Комитет считает, что для ВОЗ было бы полезным проведение специального форума для обзора последних достижений в области рационального использования ЛС.
В этой связи Комитет рекомендовал ВОЗ изменить его название и вместо «Комитет экспертов ВОЗ по использованию ОЛС» (WHO Expert Committee on the Use of Essential Drugs) присвоить ему название «Комитет экспертов ВОЗ по отбору и использованию ОЛС» — WHO Expert Committee on the Selection and Use of Essential Medicines.
4.2. Определение основных лекарственных средств
 |
В 1975 г. Всемирная ассамблея здравоохранения издала резолюцию WHA28.66, в которой обратилась к Генеральному директору ВОЗ с просьбой рекомендовать странам-участницам осуществлять «отбор и закупку основных лекарственных средств приемлемой стоимости и установленного качества в соответствии с потребностями национальных систем здравоохранения» (WHA28.66. Prophylactic and therapeutic substances. Опубликовано в: Handbook of resolutions and decisions of the World Health Assembly and the Executive Board, Volume II, 1973-1984. Geneva, World Health Organization, 1985:129). Впоследствии в резолюции WHA31.32 от 1978 г. подчеркивалась «необходимость в обеспечении достаточными количествами основных лекарственных средств надлежащего качества и приемлемой стоимости для удовлетворения потребностей стран в области здравоохранения» и провозглашалась цель — «обеспечить доступ всего населения к основным лекарственным средствам по той стоимости, которая соответствует возможностям страны» (WHA31.32. Action programme on essential drugs. Опубликовано в: Handbook of resolutions and decisions of the World Health Assembly and the Executive Board, volume II, 1973-1984. Geneva, World Health Organization, 1985:129–130).
Во время первого заседания в 1977 г. Комитет экспертов ВОЗ по отбору основных лекарственных средств дал определение ОЛС как лекарственных препаратов, которые «относятся к числу особо важных и являются основными, незаменимыми и необходимыми для охраны здоровья населения» (The selection of essential drugs. Report of a WHO Expert Committee. Geneva, World Health Organization, 1977; WHO Technical Report Series, № 615). В 1982 г. на третьем заседании Комитет экспертов ВОЗ пересмотрел определение ОЛС, которое стало звучать так: «лекарственные средства, которые удовлетворяют потребностям охраны здоровья большинства населения, поэтому они должны постоянно быть в наличии в необходимых количествах, в соответствующих лекарственных формах» (The use of essential drugs. Report of a WHO Expert Committee. Geneva, World Health Organization, 1983; WHO Technical Report Series, № 685). Это определение было утверждено и использовалось в ходе всех последующих заседаний Комитета вплоть до 1999 г.
На заседании, состоявшемся в 1999 г., Комитет принял решение объединить указанное определение с концепцией экономической доступности, провозглашенной в резолюции WHA31.32, после чего определение ОЛС стало звучать следующим образом: «лекарственные средства, удовлетворяющие потребностям охраны здоровья большинства населения, поэтому они должны постоянно быть в наличии в необходимых количествах, в соответствующих лекарственных формах и по цене, доступной для отдельных лиц и для общества в целом» (The use of essential drugs. Ninth report of the WHO Expert Committee. Geneva, World Health Organization, 2000; WHO Technical Report Series, № 895). Это определение было использовано в информационном письме, направленном в Исполнительный комитет ВОЗ в мае 2001 г.
Большинство рецензентов, принявших в 2001 г. участие в обсуждении предложенных новых процедур по пересмотру Примерного перечня ВОЗ (см. раздел 3.1.; «Еженедельник АПТЕКА», № 28 (399) от 28 июля 2003 г. — Прим. переводчика), выразили удовлетворение определением ОЛС, принятым в 1999 г. Однако некоторые участники дискуссии поставили под сомнение целесообразность включения в определение ОЛС фразы о ценовой доступности, другие высказывали замечания в отношении формулировки «большинство населения». Кроме того, высказывались сомнения относительного того, что в данном определении ОЛС исчерпывающе отражены необходимость в финансовой поддержке для обеспечения населения ОЛС и необходимость обеспечения надлежащего качества в отношении собственно ОЛС.
В отчете, который секретариат ВОЗ направил Исполнительному Комитету ВОЗ в январе 2002 г. (WHO medicines strategy revised procedure for updating WHO’s Model List of Essential Drugs. Geneva, World Health Organization, 2002 (документ EB109/8; доступен в Интернете: ), указывалось, что определение ОЛС должно включать три составляющих: формулировку, описание критериев отбора и описание конечных целей, для достижения которых разрабатывается Примерный перечень ОЛС ВОЗ (см. блок).
|
Таким образом, формулировка ОЛС соответствует таковой, принятой на первом заседании Комитета, состоявшемся в 1977 г.: ОЛС — это препараты, которые «относятся к числу особо важных и являются основными, незаменимыми и необходимыми для охраны здоровья населения». А конечная цель Примерного перечня ОЛС ВОЗ была провозглашена Комитетом в ходе его третьего заседания, состоявшегося в 1982 г.: «… поэтому они должны постоянно быть в наличии в необходимых количествах, в соответствующих лекарственных формах». Определение ОЛС и заложенный в нем конечный результат использовали для представления сути концепции ОЛС в ходе всех последующих заседаний Комитета экспертов ВОЗ.
В отчете Исполнительному комитету ВОЗ (2001 г.) секретариат подчеркнул значение еще одного элемента, который пока не нашел отражения в используемом сегодня определении ОЛС, а именно необходимость для стран и учреждений разрабатывать собственные перечни ОЛС. Как отмечалось на заседании Комитета экспертов ВОЗ, состоявшемся в 1999 г., «концепция ОЛС … предполагает гибкость и приспособляемость к различным обстоятельствам; вопрос о том, какие ЛС должны рассматриваться как основные, решается исключительно на национальном уровне».
Проведение открытой сессии позволило Комитету более тщательно изучить широкий спектр мнений о том, каким должно быть определение ОЛС. По мнению нескольких участников открытой сессии, термин «распространенность заболевания» (согласно действующему положению, отбор ОЛС осуществляется «на основании данных о распространенности заболевания, доказательных данных об эффективности и безопасности, сравнительных данных о рентабельности препарата») не учитывает сферу применения ЛС в целях профилактики и планирования семьи. Они считают, что сфера применения ЛС в профилактических целях должна быть отражена в определении ОЛС — в его части, которая посвящена критериям отбора.
Комитет одобрил предложения, высказанные в ходе открытой сессии по поводу определения ОЛС, и рекомендовал заменить термин «распространенность заболеваний» выражением «значимость для общественного здравоохранения» — в части, касающейся критериев отбора препаратов с добавлением выражения «в сопровождении адекватной информации» — в части, посвященной конечным целям, и понятия «внедрение» — в последнем предложении определения ОЛС. С учетом этих исправлений и добавлений полное определение ОЛС таково:
К основным лекарственным средствам относятся препараты, которые удовлетворяют приоритетным потребностям охраны здоровья населения. Их отбор осуществляется с надлежащим учетом значимости для общественного здравоохранения, доказательных данных об эффективности и безопасности, сравнительных данных об экономической эффективности (рентабельности) препаратов. В рамках функционирования системы здравоохранения ОЛС должны постоянно быть в наличии в необходимых количествах, в соответствующих лекарственных формах, обладать проверенным качеством, сопровождаться адекватной информацией, и иметь цену, которая делает их доступными для отдельных лиц и для общества в целом. Внедрение концепции ОЛС предполагает гибкость и приспособляемость к различным обстоятельствам; вопрос о том, какие ЛС должны рассматриваться как основные, решается исключительно на национальном уровне.
4.3. Значение стоимости лечения в отношении Примерного перечня
С тех пор как в 1975 г. были провозглашены концепция национальной лекарственной политики и концепция ОЛС, вопрос о стоимости ЛС вызывает особую озабоченность стран — участниц ВОЗ. В ходе консультаций, проводившихся на протяжении 2001 г., некоторые участники затрагивали вопросы, связанные с использованием информации о стоимости и рентабельности препаратов в процессе отбора ОЛС, а именно:
• Может ли высокая стоимость препарата послужить препятствием для его внесения в Примерный перечень ОЛС ВОЗ, если препарат соответствует критериям отбора в отношении потребности (то есть если препарат необходим для решения приоритетных проблем здравоохранения), эффективности (в сравнении с другими ЛС, используемыми для лечения того же патологического состояния) и безопасности.
• Может ли иметь практическое значение сравнение рентабельности различных препаратов для лечения отдельных патологических состояний, проведенное в мировом масштабе — с учетом значительных различий в стоимости и изменчивости цен на препараты.
На открытой сессии подчеркивалось, что сбор информации о ценах на ЛС и ее использование требуют осторожности, поскольку она быстро устаревает. Признано также, что для отбора ОЛС необходима только индикационная информация о ценах на ЛС, которая базируется на сравнении цен на препараты, относящиеся к той или иной фармакотерапевтической группе. Кроме того, информацию о текущих ценах на ЛС не всегда легко получить.
Что касается критериев отбора, то согласно новым процедурам:
• Абсолютная стоимость препарата не может служить причиной для его исключения из Примерного перечня, если он соответствует установленным критериям отбора.
• Сравнительный анализ рентабельности ЛС следует проводить в рамках одной фармакотерапевтической группы (например, определение наиболее экономически эффективного медикаментозного лечения, направленного на предотвращение передачи ВИЧ-инфекции от матери плоду).
Этот подход совпадает с принятой ВОЗ практикой, когда при разработке рекомендаций для общественного здравоохранения принимается во внимание стоимость препаратов.
Комитет отметил, что определить влияние изменения цен при подсчете рентабельности можно, воспользовавшись информацией об индикационных ценах на препараты, которая в настоящее время доступна в системе Объединенных Наций — Международное справочное руководство (International Drug Price Indicator Guide), подготовленное организацией «Management Sciences for Health» в сотрудничестве с ВОЗ. Кроме того, при необходимости следует прибегать к анализу соотношения «стоимость/польза» и проводить систематические обзоры. Комитет выразил надежду, что со временем опыт проведения анализа экономической эффективности пригодится странам — участницам ВОЗ для дальнейшего совершенствования новых процедур.
4.4. Внесение дополнительных продуктов в Примерный перечень
В настоящее время в состав Примерного перечня ОЛС ВОЗ входит большое количество препаратов, в том числе вакцины, диагностические средства, сыворотки, иммуноглобулины, а также ряд нефармацевтических средств назначения (например, инсектицидные средства и др.). По мнению Комитета, внесение этих продуктов в Примерный перечень дает повод для подачи множества заявок о внесении в Перечень подобных средств, что потребует значительных дополнительных усилий в той области, где доминируют личные предпочтения, а объективных данных для сопоставления недостаточно.
Комитет разработал общий принцип, согласно которому для внесения в Примерный перечень может рассматриваться любой продукт, являющийся предметом регуляторного контроля. Как правило, такие продукты являются предметом клинических исследований по изучению эффективности и безопасности, результаты которых рассматриваются Комитетом как достаточно надежные для проведения оценки. К этой категории могут быть отнесены продукты, подлежащие введению в человеческий организм: контрастные и другие средства для инвазивной диагностики, внутриматочные противозачаточные средства, вакцины, сыворотки, иммуноглобулины. Очевидно, должны остаться в Примерном перечне и некоторые другие продукты, давно в него включенные (например, презервативы). Однако для заявок о включении новых продуктов необходимо использовать более прагматичный подход. В этой связи Комитет предложил разработать специальный механизм и соответствующие процедуры для определения и оценки основных изделий и технологий медицинского назначения.
Запрос о создании в рамках Библиотеки ВОЗ по ОЛС гиперссылки на информацию о комплектах диагностических тестов для ВИЧ/СПИДа был возвращен в секретариат ВОЗ для повторного рассмотрения. Комитет одобрил выдвинутое Департаментом вакцин и иммунобиологических препаратов ВОЗ предложение о том, что со временем, в ходе использования Консультативными комитетами Департамента прозрачных процедур пересмотра, будут выработаны текущие рекомендации в формате, совместимом с Примерным перечнем ОЛС ВОЗ. Этот проектный перечень вакцин вместе с соответствующим обоснованием будет направлен в Комитет экспертов ВОЗ для рассмотрения вопроса о присоединении к Примерному перечню ОЛС в качестве отдельной его части. Комитет также рекомендовал включить в систематический обзор основные вакцины для использования у детей, а также вакцины комбинированного состава.
Комитет отметил, что неправильное применение растворов для инъекций является серьезной и широко распространенной проблемой, которая требует решения на различных уровнях. При широком использовании парентерального введения препаратов следует стремиться к его ограничению путем разработки и выполнения клинических рекомендаций, а также обучить медицинских работников и потребителей. Препараты для парентерального введения должны поставляться в комплекте с оборудованием, которое необходимо для обеспечения стерильных условий при проведении инъекций.
Продолжение в следующих номерах «Еженедельника АПТЕКА»
* Продолжение. Начало см. «Еженедельник АПТЕКА», № 28 (399) от 28 июля 2003 г.

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим