 Поява COVID-19 спричинила безпрецедентні зриви у проведенні клінічних досліджень та наданні медичної допомоги в усьому світі. Близько 1 тис. організацій повідомили про зриви у проведенні досліджень, починаючи з січня 2020 р., що конвертувалося у зменшення приблизно на 80% кількості нових пацієнтів, залучених у проведення клінічних досліджень, станом на квітень 2020 р. порівняно з квітнем 2019 р. З усіх активних клінічних досліджень, відповідно до даних ClinicalTrials.gov, 13% повідомили про збільшення тривалості проведення досліджень у березні–травні 2020 р. порівняно з 9% за аналогічний період 2019 р.
Поява COVID-19 спричинила безпрецедентні зриви у проведенні клінічних досліджень та наданні медичної допомоги в усьому світі. Близько 1 тис. організацій повідомили про зриви у проведенні досліджень, починаючи з січня 2020 р., що конвертувалося у зменшення приблизно на 80% кількості нових пацієнтів, залучених у проведення клінічних досліджень, станом на квітень 2020 р. порівняно з квітнем 2019 р. З усіх активних клінічних досліджень, відповідно до даних ClinicalTrials.gov, 13% повідомили про збільшення тривалості проведення досліджень у березні–травні 2020 р. порівняно з 9% за аналогічний період 2019 р.З метою гарантування безпеки пацієнтів та добросовісності проведення досліджень, фармацевтична промисловість доклала значних зусиль для пришвидшення впровадження інновацій у процес проведення клінічних досліджень, таких як цифрові інструменти та віртуалізація, що стало можливим у тому числі завдяки підтримці регуляторних органів, які розробили ряд настанов. Аналіз даних ClinicalTrials.gov у період з січня по липень 2020 р. дозволяє оцінити темпи відновлення сфери клінічних досліджень після зривів, спричинених пандемією COVID-19, та наслідків для їх подальшого проведення.
Відновлення активності клінічних досліджень
Дані ClinicalTrials.gov свідчать про зменшення кількості нових клінічних досліджень з січня по травень і подальше відновлення у червні та липні до показників, характерних для січня (рис. 1, 2). Подібним чином після сплеску в лютому та березні кількість досліджень, призупинених через COVID-19, стабілізувалася на рівні близько 1200, і призупинення почали скасовувати, причому червень став першим місяцем, коли було відмінено більше тимчасових зупинок досліджень, ніж оголошено про нові зупинки (рис. 3).
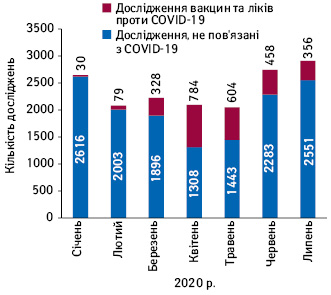
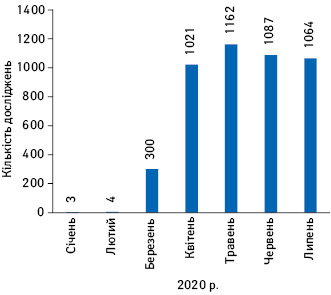
З іншого боку, не всі дані щодо клінічних досліджень такі оптимістичні. Так, відповідно до даних аналітичної компанії «Medidata» кількість нових пацієнтів у розрахунку на кожен сайт дослідження у серпні зменшилася на 20% порівняно з аналогічним показником до початку пандемії COVID-19 (тут і далі середній показник за перші 11 міс 2019 р.) та на 10% порівняно з липнем 2020 р. Слід зазначити, що аналіз «Medidata» охоплює 5222 дослідження, 198 120 сайтів.
Темпи відновлення сфери клінічних досліджень значно варіюють залежно від регіону та рівня технічного обслуговування, що пов’язано з різним впливом хвороби, а також політики у сфері охорони здоров’я та обмежень, зумовлених пандемією, що змінюються з часом.
Так, стабільне покращення ситуації з проведенням клінічних досліджень серед європейських країн впродовж квітня–серпня відмічено у Великобританії та Німеччині. Так, у Великобританії зниження рівня залученості пацієнтів скоротилося з –60% у липні до –40% у серпні порівняно з базовим рівнем до пандемії COVID-19 (рис. 4). У Німеччині у серпні навіть було відмічено зростання порівняно із докризовим рівнем. І навпаки, ситуація у Франції та Іспанії погіршилася в серпні порівняно з липнем, що відбувалося на тлі різкого збільшення кількості випадків захворювання на COVID-19. Аналогічна ситуація виявлена і в Італії, де кількість залучених у дослідження пацієнтів у серпні скоротилася до рівня квітня–травня.
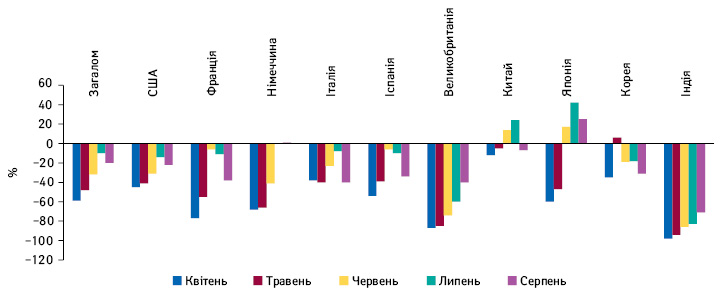
В Азії спостерігається відчутне покращення, яке розпочалося в червні у Китаї та Японії і зберігалося в липні, а в Японії — і в серпні. Втім, у Південній Кореї в серпні виявлено зменшення кількості залучених пацієнтів. Натомість в Індії виявлено тренд до повільного відновлення.
У США в серпні також зафіксовано незначне зменшення кількості нових пацієнтів, які включені у дослідження, порівняно з липнем, незважаючи на зниження рівня захворюваності на COVID-19 порівняно з липнем. Цікаво, що вперше за кілька місяців у серпні клінічні дослідження за напрямком онкології в США зазнали зменшення кількості нових пацієнтів на 10% від базового рівня до пандемії COVID-19.
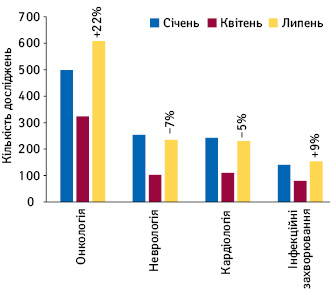
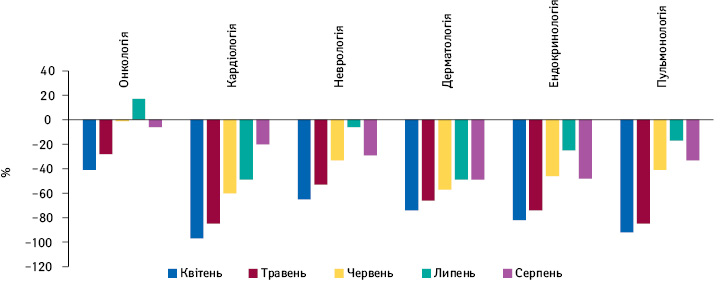
У глобальному контексті у розрізі терапевтичного напрямку клінічних досліджень вплив пандемії також відрізнявся. Втім, більшість терапевтичних напрямків стикнулися зі зменшенням кількості нових пацієнтів у серпні, включаючи онкологію — подібно до раніше виявленого для напрямку кардіології в США, однак у серпні відмічено поліпшення від –49% у липні до –20% у серпні порівняно з вихідним рівнем до пандемії COVID-19 (рис. 5). Загалом неонкологічні терапевтичні напрямки зазнали скорочення залучення пацієнтів у серпні на 31% порівняно із базовим рівнем до пандемії COVID-19.
Інновації в організації процесів під час клінічних досліджень
У травні 2020 р. було проведено опитування 245 дослідників, що беруть участь у клінічних дослідженнях, та координаторів досліджень з усього світу. Далі будуть наведені результати цього аналізу, що були опубліковані в журналі «Nature» (Xue J.Z. et al., 2020), та обговорення поточних проблем у сфері клінічних досліджень та нововведень, спрямованих на їх вирішення.
Опитування дослідників, що беруть участь у клінічних дослідженнях, було проведено приблизно на початку періоду відновлення у сфері клінічних досліджень (8–18 травня), коли лише 39% досліджень продовжувалися, як планувалося. Однак 73% дослідників (65% у США; 76% у ЄС) уже вважали, що пік кризи минув, і 80% очікували, що призупинені дослідження відновляться протягом 2 міс.
COVID-19 змінив проведення поточних досліджень, при цьому дослідники повідомляли, що 57% взаємодій з пацієнтами та 79% взаємодій між спонсорами та контрактними дослідницькими організаціями (КДО) відбуваються віддалено. Оскільки кількість особистих візитів пацієнтів у рамках досліджень зменшилася, представники фармкомпаній та регуляторні органи передбачали ризик втрати даних. У відповідь регуляторні органи розробили рекомендації щодо підходів, спрямованих на зменшення наслідків для статистичних даних, тоді як спонсорські організації застосовували засоби телемедицини та дистанційного моніторингу пацієнтів, щоб замінити особисті обстеження дослідниками та обмежити прогалини в даних.
Слід відмітити, що є ознаки того, що впровадження таких інновацій може бути тривалим. Дослідники очікують, що віддалені взаємодії пацієнта та спонсора — КДО будуть зберігатися на вищому рівні, ніж до кризи. Серед дослідників 46–78% очікують, що впровадження цифрових технологій для залучення пацієнтів продовжить зростання і після завершення кризи. Зі зміною норм залучення пацієнтів 34–52% очікують на розширення використання підходів для децентралізації досліджень, таких як нові моделі сайтів, набір пацієнтів через мережу Інтернет, домашній догляд та прямі поставки кандидатів у препарати пацієнтам.
Раніше ці типи інновацій сприймалися досить неоднозначно і в деяких випадках залишалися менш перевіреними. Наприклад, дистанційне спостереження було визнано найменш ефективним серед 5 ініціатив із залучення пацієнтів в опитуванні 2016 р., і зовсім недавно, у листопаді 2019 р., менше 40% компаній очікували, що віртуальні дослідження стануть головною складовою їх портфоліо.
Виклики клінічним дослідженням
У міру відновлення клінічної діяльності спонсори та інші зацікавлені сторони стикаються з проблемами на існуючих та нових напрямках досліджень.
Конкуренція. Оскільки щомісяця запускаються сотні досліджень кандидатів у вакцини та препаратів проти COVID-19, та більше 1000 призупинених раніше досліджень зараз повертаються до активної роботи, спонсори стикаються із жорсткою конкуренцією за потужності сайтів для проведення досліджень, дослідників та час представників регуляторних органів, що вимагає ретельного попереднього планування, активного локального моніторингу, гнучкості та тісного партнерства із сайтами та пацієнтами для дотримання таймінгу дослідження.
Технологія. До кризи дистанційні підходи при проведенні досліджень були відносно рідкісними і все ще можуть залишатися дещо фрагментованими. Масштабування інновацій потребуватиме вдосконалення інфраструктури даних для спонсорів та сайтів. Більше того, у майбутньому галузь може почати узгоджувати питання, пов’язані з уніфікацією набору загальних цифрових інструментів, що змусить регуляторні органи та постачальників альтернативних технологій дослухатися до потреб галузі.
Збір даних. Нові методи збору даних ще не стали звичними явищами; наприклад, eCOA/ePRO та eSource використовували лише 48 та 14% спонсорів відповідно у 2018 р. Ці підходи все ще можуть стикатися з прогалинами в даних та іншими проблемами, що потребує суворої перевірки та стандартизації, перш ніж вони зможуть замінити існуючі методи.
Сайти догляду. У міру того, як дослідження рухаються додому пацієнта або в інтернет, модель роботи сайту може еволюціонувати, потенційно вводячи нових лікарів у клінічні дослідження та підтримуючи зростання менших сайтів. Примітно, що 52% дослідників очікували на зростання нових моделей сайтів, наприклад таких як аптека.
Люди. Роль та обов’язки осіб, які беруть участь у проведенні клінічних досліджень, можуть змінитися; наприклад, персонал сайту переходить до надання або нагляду за мобільними медичними послугами, або вводяться цифрові записи, що сприяють скороченню ручного введення та перевірки даних. Клінічні дослідники можуть потребувати нових можливостей, і в той же час звільнення від частини обов’язків, щоб зосередитися на більш спеціалізованій роботі.
Кроки у відповідь на нові виклики
Проблеми у сфері проведення клінічних досліджень, пов’язані з COVID-19, можуть зберігатися до тих пір, поки ефективні вакцини не стануть широкодоступними, а підходи для їх вирішення стануть значно більше застосовуватися після закінчення кризи. Тому зацікавлені сторони можуть розглянути можливість довгострокової цілісної оцінки проєкту та проведення досліджень для адаптації протягом найближчих місяців та років. Це може початися з 5 основних кроків:
- застосування дизайнерського мислення щодо особистого досвіду пацієнтів та дослідників, оптимізуючи незнайомий віртуальний досвід та навчаючись на основі відгуків у режимі реального часу;
- експерименти та зміни в пробному середовищі, швидке навчання на прикладі пілотних проєктів, після чого — проведення масштабування. Доцільно скористатися цією можливістю, щоб не просто вирішити негайну кризу, а широко впровадити інновації в запланований пробний портфель;
- розвиток екосистем з партнерами та участь у стандартизації технологій, даних та регулювання, щоб пришвидшити впровадження інновацій та зменшити навантаження на дослідників та сайти;
- вивчення більш широкого набору інструментів доказової медицини, таких як дані із рутинної практики або цифрові проспективні реєстри, щоб доповнити традиційні рандомізовані клінічні дослідження на базі сайтів;
- розширення впровадження цифрових технологій та інвестиції в управління змінами, що дозволить користувачам застосовувати нові інструменти та задіяти їх у правильному контексті.
COVID-19 продемонстрував, що спонсори та дослідники можуть досягти за тижні того, на що раніше були потрібні місяці чи роки, та підкреслив гуманітарну важливість ефективних, надійних та точних клінічних досліджень. Дії галузі протягом наступних 1–2 років можуть визначити нові правила гри у сфері клінічних досліджень лікарських засобів, даючи кожному зацікавленому учаснику можливість не лише адаптуватися, але й сформувати майбутню парадигму клінічного дослідження.
за матеріалами nature.com, medidata.com

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим