 Вступительным словом от имени министра здравоохранения Украины семинар открыл Валерий Стецив, директор Департамента регуляторной политики в сфере обращения лекарственных средств и продукции в системе здравоохранения МЗ Украины. Тепло приветствуя зарубежных коллег в Украине, он пожелал участникам плодотворной работы и отметил, что запланированные для рассмотрения на совещании вопросы крайне важны и требуют прицельного внимания со стороны как отдельных организаций, так и государства в целом. Фальсификация лекарств является проблемой международного масштаба, каждая упаковка поддельного препарата несет потенциальную угрозу здоровью и жизни граждан. Поэтому работа по решению этой проблемы требует тесного сотрудничества регуляторных органов в сфере обращения лекарственных средств разных стран, таможенных и правоохранительных органов, общества в целом. Цель встречи — обсуждение основных законодательных и регуляторных препятствий для принципиального и эффективного противодействия возрастающей угрозе распространения фальсифицированных медикаментов; налаживание координации между представителями промышленности, потребителями, неправительственными организациями, представителями государственных регуляторных учреждений и правоохранительных органов; предоставление информации о прогрессивных решениях в борьбе с угрозой распространения поддельных медикаментов. Выступающий выразил надежду, что семинар послужит усилению уверенности потребителей в том, что присутствующие на рынке лекарства являются качественными, эффективными и безопасными, будет способствовать увеличению потока инвестиций частного сектора в фармацевтическую отрасль и более строгому выполнению регуляторных правил и норм международной торговли продукцией медицинского назначения, повысит уровень компетентности и действенной консолидации усилий в выявлении и противодействии распространению поддельных лекарств.
Вступительным словом от имени министра здравоохранения Украины семинар открыл Валерий Стецив, директор Департамента регуляторной политики в сфере обращения лекарственных средств и продукции в системе здравоохранения МЗ Украины. Тепло приветствуя зарубежных коллег в Украине, он пожелал участникам плодотворной работы и отметил, что запланированные для рассмотрения на совещании вопросы крайне важны и требуют прицельного внимания со стороны как отдельных организаций, так и государства в целом. Фальсификация лекарств является проблемой международного масштаба, каждая упаковка поддельного препарата несет потенциальную угрозу здоровью и жизни граждан. Поэтому работа по решению этой проблемы требует тесного сотрудничества регуляторных органов в сфере обращения лекарственных средств разных стран, таможенных и правоохранительных органов, общества в целом. Цель встречи — обсуждение основных законодательных и регуляторных препятствий для принципиального и эффективного противодействия возрастающей угрозе распространения фальсифицированных медикаментов; налаживание координации между представителями промышленности, потребителями, неправительственными организациями, представителями государственных регуляторных учреждений и правоохранительных органов; предоставление информации о прогрессивных решениях в борьбе с угрозой распространения поддельных медикаментов. Выступающий выразил надежду, что семинар послужит усилению уверенности потребителей в том, что присутствующие на рынке лекарства являются качественными, эффективными и безопасными, будет способствовать увеличению потока инвестиций частного сектора в фармацевтическую отрасль и более строгому выполнению регуляторных правил и норм международной торговли продукцией медицинского назначения, повысит уровень компетентности и действенной консолидации усилий в выявлении и противодействии распространению поддельных лекарств.
 Как сообщил Игорь Поканевич, директор бюро ВОЗ в Украине, в сфере борьбы с НПЛФК на протяжении многих лет ведется скоординированная работа между штаб-квартирой ВОЗ, Европейским региональным бюро ВОЗ, украинским офисом организации, органами регулирования лекарственного оборота и государственными органами власти в лице МЗ Украины. На этом пути достигнуты определенные успехи, решение проблемы вынесено на высокий уровень, этому вопросу уделяют серьезное внимание первые лица государства. Об этом свидетельствует и тот факт, что буквально накануне открытия семинара, 31 мая текущего года парламент Украины принял за основу в первом чтении проект Закона Украины «О внесении изменений в некоторые законы (о противодействии фальсификации лекарственных средств)», которым предлагается внести изменения в Уголовный кодекс Украины, Уголовно-процессуальный кодекс Украины, Кодекс Украины об административных правонарушениях и Закон Украины «О лекарственных средствах» — с целью усовершенствования соответствующих нормативно-правовых актов в пользу усиления ответственности за нарушение законодательства об обороте лекарственных средств, более эффективной защиты населения от негативных последствий незаконного оборота и применения фальсифицированных (поддельных) лекарственных препаратов и изделий медицинского назначения. Выступающий выразил надежду, что среди примеров других стран, представленных в ходе работы семинара, в когорте своих европейских собратьев найдет достойное отображение и пример Украины в противодействии фальсифицированным и контрафактным лекарствам.
Как сообщил Игорь Поканевич, директор бюро ВОЗ в Украине, в сфере борьбы с НПЛФК на протяжении многих лет ведется скоординированная работа между штаб-квартирой ВОЗ, Европейским региональным бюро ВОЗ, украинским офисом организации, органами регулирования лекарственного оборота и государственными органами власти в лице МЗ Украины. На этом пути достигнуты определенные успехи, решение проблемы вынесено на высокий уровень, этому вопросу уделяют серьезное внимание первые лица государства. Об этом свидетельствует и тот факт, что буквально накануне открытия семинара, 31 мая текущего года парламент Украины принял за основу в первом чтении проект Закона Украины «О внесении изменений в некоторые законы (о противодействии фальсификации лекарственных средств)», которым предлагается внести изменения в Уголовный кодекс Украины, Уголовно-процессуальный кодекс Украины, Кодекс Украины об административных правонарушениях и Закон Украины «О лекарственных средствах» — с целью усовершенствования соответствующих нормативно-правовых актов в пользу усиления ответственности за нарушение законодательства об обороте лекарственных средств, более эффективной защиты населения от негативных последствий незаконного оборота и применения фальсифицированных (поддельных) лекарственных препаратов и изделий медицинского назначения. Выступающий выразил надежду, что среди примеров других стран, представленных в ходе работы семинара, в когорте своих европейских собратьев найдет достойное отображение и пример Украины в противодействии фальсифицированным и контрафактным лекарствам.
 В подтверждение этих слов Андрей Захараш, заместитель председателя Государственной службы Украины по лекарственным средствам (Гослекслужба), представил слушателям широкий срез многообразной работы, которая проводится в Украине в рамках системы государственного контроля качества лекарственных средств. Начав с дефинитивного уровня, он напомнил, что под категорию фальсифицированных (поддельных) подпадают те лекарственные средства, которые умышленно или обманным путем неправильно маркированы (этикетированы) в нарушение их идентичности (любая ложная информация о названии, составе, дозе или других данных о препарате) и/или касательно источника их происхождения (любая ложная информация о производителе, стране производства, стране происхождения, владельце регистрационного свидетельства).
В подтверждение этих слов Андрей Захараш, заместитель председателя Государственной службы Украины по лекарственным средствам (Гослекслужба), представил слушателям широкий срез многообразной работы, которая проводится в Украине в рамках системы государственного контроля качества лекарственных средств. Начав с дефинитивного уровня, он напомнил, что под категорию фальсифицированных (поддельных) подпадают те лекарственные средства, которые умышленно или обманным путем неправильно маркированы (этикетированы) в нарушение их идентичности (любая ложная информация о названии, составе, дозе или других данных о препарате) и/или касательно источника их происхождения (любая ложная информация о производителе, стране производства, стране происхождения, владельце регистрационного свидетельства).
Среди основных факторов, усложняющих реализацию фальсифицированных лекарственных средств через аптечную сеть, были названы:
- государственная политика по борьбе с фальсификацией лекарств,
- высокая себестоимость производства лекарственных средств,
- наличие эффективной системы защиты интеллектуальных прав,
- наличие дееспособной контролирующей и правоохранительной системы.
К кругу основных задач Гослекслужбы Украины докладчик причислил:
- обеспечение качества и безопасности лекарственных средств, в том числе закупаемых за средства государственного и местных бюджетов, в ходе их производства, хранения, транспортирования, реализации субъектами хозяйствования, в том числе и путем внедрения требований надлежащих практик, утилизации и уничтожения;
- контроль выполнения Лицензионных условий осуществления хозяйственной деятельности по производству лекарственных средств, оптовой и розничной торговле ими независимо от формы собственности и ведомственного подчинения;
- государственный контроль ввоза лекарственных средств на таможенную территорию Украины;
- осуществление государственного контроля и надзор за соблюдением требований, стандартов и технических условий при транспортировании, хранении и использовании лекарственных средств, в том числе иммунобиологических препаратов;
- отбор в установленном порядке образцов для проверки их качества;
- выдача обязательных для выполнения предписаний об устранении нарушений стандартов и технических условий, фармакопейных статей и технических регламентов, а также нарушений в ходе производства, хранения, транспортирования и реализации лекарственных средств;
- принятие в установленном порядке решений об изъятии из оборота и запрещении (остановке) производства, реализации и использования лекарственных средств, не соответствующих требованиям, определенным нормативно-правовыми актами и нормативными документами, а также тех, которые ввозятся на территорию Украины с нарушением установленного законодательством порядка.
Система контроля качества лекарственных средств в Украине подразделяется на три уровня:
1. Государственный контроль при ввозе на территорию Украины и производства в Украине.
2. Контроль уполномоченными лицами субъектов хозяйствования.
3. Контроль инспекторами территориальных органов Гослекслужбы Украины в ходе проведения плановых и внеплановых проверок субъектов хозяйствования.
Первый уровень: все лекарственные средства и продукция in bulk при ввозе на таможенную территорию Украины подлежат обязательному государственному контролю качества согласно требованиям, изложенным в постановлении КМ Украины № 902 «О Порядке осуществления государственного контроля качества лекарственных средств, которые ввозятся в Украину». Этот Порядок определяет механизм государственного контроля качества ввозимых на территорию нашей страны лекарств и осуществляется с целью недопущения оборота фальсифицированных, некачественных и незарегистрированных препаратов.
Второй уровень: в соответствии с Инструкцией о порядке контроля качества лекарственных средств в ходе оптовой и розничной торговли, утвержденной приказом МЗ Украины № 436, и положениями приказа МЗ Украины № 584 «Об утверждении правил хранения и проведения контроля качества лекарственных средств в лечебно-профилактических учреждениях», уполномоченное лицо, которое входит в штат каждого хозяйствующего субъекта, осуществляет входной контроль лекарственных средств, поступающих в аптеку, ее структурные подразделения и лечебно-профилактические учреждения.
Третий уровень: в соответствии с Законом Украины «Об основных принципах государственного контроля (надзора) в сфере хозяйственной деятельности» в ходе плановых и внеплановых проверок хозяйствующих субъектов или их обособленных подразделений органы государственного контроля проверяют их деятельность по соблюдению соответствия Лицензионным условиям. При этом органами госконтроля отбираются образцы лекарственных средств для проведения лабораторного анализа в подчиненных им лабораториях. Указанный комплекс мер сводит к минимуму возможность попадания фальсифицированных, некачественных и незарегистрированных лекарственных средств на рынок Украины. Также разработана Программа по борьбе с фальсифицированными лекарственными средствами на 2011–2016 гг., которая в настоящее время проходит согласование в заинтересованных министерствах и ведомствах.

2011 г. стал переломным и судьбоносным для украинской системы контроля качества лекарств: А. Захараш с гордостью подчеркнул, что с начала текущего года Украина является полноправным членом Международной системы сотрудничества фармацевтических инспекций (PIC/S). Для этого в предыдущие годы и особенно активно в 2010 г. была проделана значительная работа, в частности по внедрению системы качества в рамках деятельности Гослекслужбы, формированию штата GMP-инспекторов и их обучения (в том числе под эгидой PIC/S), активному сотрудничеству с регуляторными органами стран-членов PIC/S, а также международными организациями, прежде всего ВОЗ. В Гослекслужбе была внедрена система качества, разработанная в соответствии с требованиями PIC/S («Рекомендации PIC/S касательно требований к системе качества фармацевтических инспекторатов»), ВОЗ («Требования к системам качества национальных инспекторатов GMP»), национального стандарта ДСТУ ISO 9001:2009 (международного стандарта ISO 9001:2008). Нормативная база, внедряющая европейские стандарты производства лекарственных средств, а также контроля их качества и безопасности, зиждется на положениях приказа МЗ Украины от 16.02.2009 г. № 95, которым утверждены руководства по надлежащим производственной, дистрибьюторской, лабораторной и клинической практикам.
PIC/S является действенным международным инструментом взаимодействия между странами и их регуляторными органами по контролю качества лекарств (национальными фармацевтическими инспекторатами), которые совместными усилиями обеспечивают активное и конструктивное сотрудничество в сфере GMP, инспектирования и лицензирования. От прямого участия в этой авторитетной международной организации наша страна получает широкий круг преимуществ, среди которых:
- уменьшение количества инспекций — участие национального уполномоченного регуляторного органа Украины в PIC/S позволит избежать многочисленных инспекций отечественных предприятий зарубежными инспекторами;
- расширение экспортных возможностей — результаты инспектирования признаются при регистрации лекарственных средств в странах — членах PIC/S, что существенно упрощает доступ отечественных производителей на внешние рынки;
- укрепление сотрудничества между уполномоченными органами в сфере инспектирования и содействие обеспечению его качества, обмен информацией и опытом между уполномоченными контрольно-регуляторными органами, координация подготовки инспекторов и экспертов;
- содействие гармонизации национальных требований GМР, совершенствование и гармонизация стандартов и процедур для инспектирования производителей лекарственных средств, взаимное признание сертификатов соответствия производства лекарственных средств требованиям GМР.
К основным источникам поступления фальсифицированных лекарственных средств на фармрынок Украины докладчик причислил контрабандные поставки производителями и реализаторами лекарственных средств из-за рубежа под видом других товаров, переупаковку просроченных лекарственных средств с целью последующей реализации, выпуск фальсифицированных лекарственных средств неустановленными предприятиями с использованием высокотехнологического оборудования и привлечением квалифицированных специалистов. Был упомянут яркий пример эффективного взаимодействия Гослекслужбы с правоохранительными органами, в ходе которого был выявлен и ликвидирован масштабный источник «качественного» доморощенного фальсификата — подпольный цех в Василькове Киевской обл., где были найдены и впоследствии уничтожены десятки тысяч упаковок подделок некоторых успешно продаваемых на украинском рынке импортных препаратов. Согласно озвученным данным о результатах работы Гослекслужбы за 2010 г., всего было издано 385 предписаний о запрещении реализации (торговли), хранения и использования лекарственных средств, в том числе 145 предписаний о запрещении 388 серий 116 наименований некачественных лекарственных средств, 43 — касательно 77 серий 29 наименований фальсифицированных препаратов, 197 — в отношении 265 наименований незарегистрированных лекарственных средств. Приказом Гослекслужбы была создана постоянно действующая рабочая группа по отслеживанию путей распространения фальсифицированных лекарственных средств, субстанций, ввозимых на территорию Украины, движения использованного и списанного технологического оборудования, которое может быть задействовано для изготовления фальсифката.
А. Захараш бегло очертил основные приоритетные перспективы деятельности ведомства, среди которых:
- содействие принятию во втором чтении закона относительно усиления ответственности за фальсификацию лекарственных средств;
- подписание меморандумов о взаимопонимании с регуляторными органами в сфере оборота лекарств Китая и Индии;
- с целью оперативного выявления фальсифицированных лекарственных средств: закупка инфракрасных спектрофотометров ближнего действия, создание и постоянное обновление библиотеки данных инфракрасных спектров;
- дооснащение 20 контрольно-аналитических лабораторий на базе территориальных органов Гослекслужбы и доведение их до уровня, отвечающего современным требованиям, предъявляемым к физико-химическим и химическим лабораториям по контролю качества лекарственных средств;
- закупка для территориальных органов государственного контроля качества лекарственных средств оборудования, позволяющего проводить экспресс-тестирование идентичности лекарственных средств в любых условиях, что позволит существенно увеличить долю выявления НПЛФК в ходе проверок хозяйствующих субъектов;
- подписание Конвенции Совета Европы по фальсификации медицинской продукции и других правонарушений, угрожающих здоровью населения;
- реализация стратегии интеграции Украины в Европейское сообщество путем гармонизации законодательного и нормативно-правового регулирования и контроля сферы оборота лекарственных средств и изделий медицинского назначения;
- усовершенствование единой информационной системы оборота лекарственных средств;
- систематическое повышение квалификации государственных инспекторов путем проведения международных семинаров, конференций, курсов;
- изучение и взятие на вооружение опыта европейских стран по принятию эффективных упредительных мер, позволяющих поставить надежные заслоны на пути проникновения НПЛФК.
 В заключение доклада А. Захараш тепло поблагодарил ВОЗ за те конструктивные предложения и технические решения, бесценную экспертную и интеллектуальную поддержку, которые украинские специалисты в сфере лекарственного оборота получают от Организации.
В заключение доклада А. Захараш тепло поблагодарил ВОЗ за те конструктивные предложения и технические решения, бесценную экспертную и интеллектуальную поддержку, которые украинские специалисты в сфере лекарственного оборота получают от Организации.
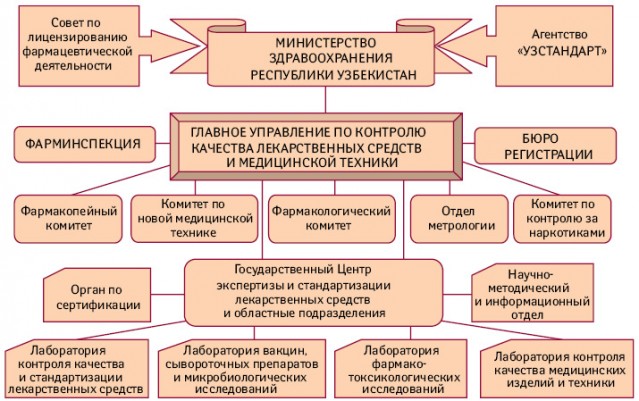
Вслед за своим украинским коллегой о состоянии работы по предотвращению поступления в обращение фальсифицированных лекарственных средств в Республике Узбекистан поведал Исмаджан Азизов, профессор, доктор фармацевтических наук, первый заместитель начальника Главного управления по контролю качества лекарственных средств и медицинской техники Министерства здравоохранения Республики Узбекистан, начальник республиканской Фарминспекции. Он рассказал о структуре системы контроля качества лекарств в Узбекистане (рисунок) и отметил, что в последнее время в стране были сделаны серьезные шаги по укреплению законодательства по борьбе с НПЛФК — прежде всего, благодаря принятию в 2009 г. государственного Плана мероприятий по систематизации работы, направленной на предотвращение поступления в обращение некачественной и фальсифицированной продукции, и контролю за обеспечением медицинских учреждений лекарственными средствами.
Так, если до утверждения данного Плана в законодательстве отсутствовали четкие критерии, определяющие понятия «фальсифицированное лекарственное средство», «недоброкачественное лекарственное средство», а также отсутствовали статьи, запрещающие реализацию, производство фальсифицированных лекарственных средств (что не позволяло создать надежный барьер для неофициального поступления через границы республики фальсифицированной медицинской продукции), то после его принятия были разработаны и внесены в установленном порядке изменения и дополнения в Закон Республики Узбекистан «О лекарственных средствах и фармацевтической деятельности». В нем нашли отображение некоторые важные дефиниции:
- «фальсифицированное лекарственное средство — лекарственное средство, сопровождаемое ложной информацией о составе и (или) производителе»;
- «недоброкачественное лекарственное средство — лекарственное средство, пришедшее в негодность, и (или) лекарственное средство с истекшим сроком годности»,
и принципиальные положения:
- «Запрещается производство лекарственных средств, не прошедших государственную регистрацию в Республике Узбекистан, фальсифицированных лекарственных средств»;
- «Запрещается реализация фальсифицированных и незарегистрированных в Республике Узбекистан лекарственных средств»;
- «Запрещается реализация и использование недоброкачественных средств»;
- «Запрещается импорт на территорию Республики Узбекистан недоброкачественных или фальсифицированных лекарственных средств».
Были также разработаны и внесены в установленном порядке изменения и дополнения в Кодекс Республики Узбекистан об административной ответственности:
«Производство, изготовление, приобретение, хранение, перевозка в целях сбыта или сбыт недоброкачественных либо фальсифицированных лекарственных средств или изделий медицинского назначения влечет наложение штрафа от пятидесяти до ста минимальных размеров заработной платы с конфискацией орудий и предметов совершения указанных правонарушений».
В целях предотвращения нелегального поступления на потребительский рынок страны некачественных/непригодных для использования лекарственных средств, создающих угрозу для здоровья и жизни граждан, были разработаны и внесены в установленном порядке изменения и дополнения в Уголовный кодекс Республики Узбекистан:
«Производство, изготовление, приобретение, хранение, перевозка в целях сбыта или сбыт недоброкачественных либо фальсифицированных лекарственных средств или изделий медицинского назначения, совершенные после применения административного взыскания за такие же действия, наказывается штрафом от ста до трехсот минимальных размеров заработной платы или исправительными работами до трех лет либо лишением свободы до трех лет .
Производство, изготовление, приобретение, хранение, перевозка в целях сбыта или сбыт недоброкачественных либо фальсифицированных лекарственных средств или изделий медицинского назначения:
а) совершенное в крупном размере;
б) совершенное по предварительному сговору группой лиц;
в) совершенное повторно или опасным рецидивистом;
г) совершенное путем злоупотребления должностным положением;
д) повлекшее средней тяжести или тяжкое телесное повреждение;
е) совершенное путем подделки документов, удостоверяющих качество и государственную регистрацию лекарственных средств или изделий медицинского назначения,
наказывается лишением свободы от трех до семи лет.
Производство, изготовление, приобретение, хранение, перевозка в целях сбыта или сбыт недоброкачественных либо фальсифицированных лекарственных средств или изделий медицинского назначения:
а) совершенное в особо крупном размере;
б) совершенное организационной группой или в ее интересах;
в) повлекшее смерть человека;
г) повлекшее иные тяжкие последствия,
наказывается лишением свободы от семи до пятнадцати лет».

Кроме того, в целях предупреждения нарушения установленных правил закупки, хранения и реализации лекарственных средств и изделий медицинского назначения хозяйствующими субъектами, имеющими лицензию на фармацевтическую деятельность:
- усилена работа по надзору за качеством лекарственных средств в аптечных учреждениях и на фармацевтических предприятиях;
- повсеместно проводятся профилактические работы с хозяйствующими субъектами, имеющими лицензию на фармацевтическую деятельность;
- во всех областях республики организованы «дни открытых дверей»;
- организованы «телефоны доверия», по которым хозяйствующие субъекты могут задать интересующие их вопросы;
- ежеквартально информация о выявленных фальсифицированных и некачественных препаратах публикуется в журнале «Фармацевтический вестник Узбекистана»;
- в целях повышения информированности населения, лицензиатов и соответствующих уполномоченных органов о выявленных фальсифицированных, некачественных лекарственных средствах и проводимой в данном направлении работе создан официальный сайт, где ежеквартально публикуется данная информация: www. uzpharm-control.uz.
Активно проводится совместнаяработа с правоохранительными органами и их территориальными подразделениями:
- Генеральной прокуратурой;
- Департаментом прокуратуры по борьбе с налоговыми и валютными преступлениями;
- Службой национальной безопасности;
- Министерством внутренних дел;
- Государственным налоговым комитетом;
- Государственным таможенным комитетом.
Создан целый ряд предпосылок и условий для предотвращения ввоза фальсифицированной медицинской продукции в Республику Узбекистан. В целях контроля внутреннего рынка и предотвращения незаконного оборота фальсифицированных лекарственных средств и некачественных изделий медицинского назначения в республике созданы оперативные группы контроля, состоящие из представителей Министерства здравоохранения, Государственного налогового комитета, Государственного таможенного комитета, Министерства внутренних дел, Антимонопольного комитета. Ежеквартальный отчет о работе этих оперативных групп предоставляется в Кабинет Министров. Используются современные аппаратура и физико-химические методы анализа при проведении контроля качества лекарственных средств по показателям «Количественное определение», «Подлинность» и «Примеси». Серьезным препятствием на пути ввоза НПЛФК на территорию республики является обязательная сертификация медицинской продукции. Полезным пособием в борьбе по предотвращению поступления на фармацевтический рынок страны НПЛФК служат разработанные и активно используемые «Методические рекомендации по выявлению фальсифицированных лекарств», которые помогают отличить подлинный препарат от фальсифицированного. Создана комплексная база данных по фальсифицированным и забракованным лекарственным средствам для районных аптечных учреждений, филиалов региональных лабораторий государственного центра экспертизы и стандартизации лекарственных средств Главного управления по контролю качества лекарственных средств и медицинской техники. Республика Узбекистан принимает активное участие в Программе ВОЗ по международному мониторингу безопасности лекарственных средств.
В заключение доклада профессор И. Азизов выразил глубокую благодарность в адрес Европейского регионального бюро ВОЗ и непосредственно его сотруднику, курирующему фармацевтическую деятельность в странах СНГ, Нине Саутенковой за многолетнюю важную экспертную и техническую помощь в ходе уже проведенных и проводимых далее реформ по реконструктивному усовершенствованию системы контроля качества лекарств в Республике Узбекистан.
По завершении семинара состоялась пресс-конференция, в которой приняли участие представители отечественных органов регулирования лекарственных средств — Андрей Захараш, заместитель председателя Гослекслужбы Украины, Сергей Дубовицкий, директор департамента организации государственного контроля качества Гослекслужбы Украины; штаб-квартиры ВОЗ (Женева) — д-р Сабине Копп, руководитель программы по обеспечению качества лекарственных средств и противодействию поддельной фармацевтической продукции, д-р Самвел Азатян, руководитель Программы поддержки национальных регуляторных органов; Европейского регионального бюро ВОЗ (Коппенгаген) — Киз де Йонкере, региональный советник по технологиям здравоохранения и лекарственным средствам, Нина Саутенкова, ответственный сотрудник по работе в сфере лекарственных средств в новых независимых государствах.
Основной целью семинара было установить интерес стран к участию в проекте под эгидой ВОЗ, который будет направлен на выявление НПЛФК в государствах европейского региона, создание ими единого методологического подхода к решению болезненной международной проблемы фальсификации лекарственных средств. Н. Саутенкова охарактеризовала результаты работы семинара как успешные, а цель — как достигнутую: заинтересованность в проекте высказали все страны, участвовавшие в семинаре. Теперь в этом направлении предстоит последующая работа: вначале будут отобраны пилотные страны, затем создан и воплощен план вовлечения в проект остальных государств региона. Проблема фальсификации лекарств существует давно и не первый год находится в фокусе внимания ВОЗ, где создана специальная рабочая группа (International Medical Products Anti-Counterfeiting Taskforce — IMPACT; www.who.int/impact/en) по противодействию НПЛФК, руководимая д-ром С. Копп. Отдельные государства не могут в одиночку побороть глобальную проблему, и с помощью проекта ВОЗ, имеющего четкие задачи и планы, среди стран европейского региона будет инициировано международное сотрудничество по противодействию НПЛФК.
По словам д-ра С. Азатяна, данный проект, фактически, уже начат, на первых порах его планируется развернуть в двух регионах — Европейском и Западно-Тихоокеанском. Предварительно продолжительность проекта исчисляется 4–5 годами. Однако очевидно, что эти сроки приблизительны и обусловлены только наличием конкретной программы ВОЗ, а затем страны перехватят эстафету и будут продолжать совместную работу самостоятельно. Сегодня же задача ВОЗ состоит в том, чтобы инициировать сотрудничество между странами, наладить их взаимопонимание, вложить им в руки общие методологические ключи. Сама же деятельность по санации лекарственного оборота от подделок и искоренению этого сверхприбыльного преступного международного бизнеса не может быть ограничена временными рамками или государственными границами, — она должна вестись перманентно и системно консолидированными и скоординированными усилиями регуляторных, правоохранительных, таможенных и других органов государственной власти разных стран.
Кроме стран Восточной, Юго-Восточной Европы и Средней Азии в семинаре приняли участие эксперты, представляющие регуляторные органы США, Великобритании, Нидерландов, ряда стран ЕС, а также Совет Европы. По мнению К. де Йонкере, их доклады подтвердили, что проблема фальсификации лекарств носит действительно глобальный характер и затрагивает все страны без разбора: и бедные, и богатые. Это значит, что побороть эту проблему в каждой отдельной стране невозможно, а возможно — только путем обмена опытом между странами. НПЛФК не только подвергает риску здоровье пациентов, но и подрывает доверие граждан к системе здравоохранения в целом. Губительность проблемы фальсификации лекарств заключается в ее скрытости от глаз людских, в том, что она создает «прецедент подлога». Поэтому так важно иметь мощные, проницательные, готовые к оперативному регулированию регуляторные системы, способные обеспечить высокое качество, эффективность и безопасность лекарств, присутствующих на рынке.
Как убедительно засвидетельствовали прозвучавшие с трибуны семинара мнения представителей стран, располагающих наиболее развитыми системами лекарственного контроля и регулирования, — даже такие государства не застрахованы от фальшивотаблетчиков. Последние были, есть и будут, причем стремятся изобретать новые, все более изощренные методы и каналы метастазирования в лекарственный оборот: чтобы эффективно им противостоять, контрольно-регуляторные инстанции рука об руку с правоохранительными органами всегда должны быть на шаг впереди. В последующих публикациях мы вернемся к освещению работы Первого регионального семинара ВОЗ: читателя ждет фармацевтический детектив международного масштаба, схема которого была изобличена в Великобритании, обзор методов борьбы с НПЛФК, стоящих на вооружении у самого могущественного на планете регуляторного органа США — FDA, и еще много интересного.

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим